 Классификация кристаллических структур на основе локализованных в них типах химической связи Если в кристалле связь между всеми атомами одинакова, то такие структуры называют гомодесмическими (от греч. Гомо –одинаковый, десмос –связь) Если в кристалле реализуется несколько типов химической связи, такие структуры называются гетеродесмическими (от греч. гетеро – разные) На основании расположения материальных частиц в кристаллах можно выделить пять геометрически разных типов структур – структурных мотивов: координационный, островной, цепочечный, слоистый и каркасный.
Классификация кристаллических структур на основе локализованных в них типах химической связи Если в кристалле связь между всеми атомами одинакова, то такие структуры называют гомодесмическими (от греч. Гомо –одинаковый, десмос –связь) Если в кристалле реализуется несколько типов химической связи, такие структуры называются гетеродесмическими (от греч. гетеро – разные) На основании расположения материальных частиц в кристаллах можно выделить пять геометрически разных типов структур – структурных мотивов: координационный, островной, цепочечный, слоистый и каркасный.
 Плотнейшие упаковки частиц в кристаллах Постройка из атомов или ионов молекул должна обладать минимальной внутренней энергией Способ заполнения пространства шарами одинакового радиуса, при котором расстояние между центрами частиц минимальны, называются плотнейшими упаковками Гексагональная плотнейшая упаковка получается при последовательной укладке слоев с гексагональной упаковкой слоев. Шары одинакового радиуса в одном слое максимально плотно можно уложить единственным способом: каждый шар окружен в слое шестью ближайшими соседями, между ним и его соседями имеются треугольные промежутки (слой А). Второй плотно упакованной слой тоже можно получить единственным способом: (слой В), у каждого верхнего шара будут три одинаковых соседа в нижнем слое и, наоборот, каждый нижний шар будет соприкасаться с тремя верхними. В гексагональной упаковке шаров третий слой точно повторяет первый, и упаковка оказывается двухслойной и запишется как чередование двух слоев А и В: АВ АВ АВ. В кубической упаковке шаров шары третьего слоя (слой С) находятся над пустотами первого, вся упаковка трехслойная, повторение мотива наступает в четвертом слое, в буквенном обозначении запишется как АВС АВС ….
Плотнейшие упаковки частиц в кристаллах Постройка из атомов или ионов молекул должна обладать минимальной внутренней энергией Способ заполнения пространства шарами одинакового радиуса, при котором расстояние между центрами частиц минимальны, называются плотнейшими упаковками Гексагональная плотнейшая упаковка получается при последовательной укладке слоев с гексагональной упаковкой слоев. Шары одинакового радиуса в одном слое максимально плотно можно уложить единственным способом: каждый шар окружен в слое шестью ближайшими соседями, между ним и его соседями имеются треугольные промежутки (слой А). Второй плотно упакованной слой тоже можно получить единственным способом: (слой В), у каждого верхнего шара будут три одинаковых соседа в нижнем слое и, наоборот, каждый нижний шар будет соприкасаться с тремя верхними. В гексагональной упаковке шаров третий слой точно повторяет первый, и упаковка оказывается двухслойной и запишется как чередование двух слоев А и В: АВ АВ АВ. В кубической упаковке шаров шары третьего слоя (слой С) находятся над пустотами первого, вся упаковка трехслойная, повторение мотива наступает в четвертом слое, в буквенном обозначении запишется как АВС АВС ….

 В плотноупакованном пространстве можно выделить два типа пустот. Пустоты одного типа окружены четырьмя соседними шарами, а пустоты второго типа шестью. Соединив центры тяжести четырех шаров, получим тетраэдр - тетраэдрическую пустоту, во втором случае получим пустоту в форме октаэдра – октаэдрическую пустоту. Все разнообразие структур, построенных на основе плотнейших упаковок, определяют в основном катионные мотивы, т. е. тип, число и расположение занятых пустот. В методе моделирования кристаллических структур, предложенном Л. Полингом, шары, образующие плотнейшую упаковку, всегда соответствуют анионам. Если соединить центры тяжести этих шаров между собой линиями, то все плотноупакованное кристаллическое пространство разбивается на октаэдры и тетраэдры без промежутков.
В плотноупакованном пространстве можно выделить два типа пустот. Пустоты одного типа окружены четырьмя соседними шарами, а пустоты второго типа шестью. Соединив центры тяжести четырех шаров, получим тетраэдр - тетраэдрическую пустоту, во втором случае получим пустоту в форме октаэдра – октаэдрическую пустоту. Все разнообразие структур, построенных на основе плотнейших упаковок, определяют в основном катионные мотивы, т. е. тип, число и расположение занятых пустот. В методе моделирования кристаллических структур, предложенном Л. Полингом, шары, образующие плотнейшую упаковку, всегда соответствуют анионам. Если соединить центры тяжести этих шаров между собой линиями, то все плотноупакованное кристаллическое пространство разбивается на октаэдры и тетраэдры без промежутков.
 Проекция на плоскость хy кристаллической структуры оливина(Mg, Fe)2 Выделены координационные полиэдры – октаэдры – вокруг атомов Mg и Fe (М 1 и М 2) и тетраэдры вокруг атомов Si
Проекция на плоскость хy кристаллической структуры оливина(Mg, Fe)2 Выделены координационные полиэдры – октаэдры – вокруг атомов Mg и Fe (М 1 и М 2) и тетраэдры вокруг атомов Si
 Координационные числа и координационные многогранники (полиэдры) Число ближайших соседей, окружающих данную частицу в структурах кристаллов называется координационным числом. Условный многогранник, в центре которого находится частица, а вершины представлены ее координационным окружением называют координационным полиэдром.
Координационные числа и координационные многогранники (полиэдры) Число ближайших соседей, окружающих данную частицу в структурах кристаллов называется координационным числом. Условный многогранник, в центре которого находится частица, а вершины представлены ее координационным окружением называют координационным полиэдром.


 Островные структуры состоят из отдельных конечных группировок (часто молекул). В структуре кристаллического хлора, построенной из отдельных молекул Cl кратчайшее расстояние между двумя атомами Cl отвечает ковалентной связи, тогда как минимальное расстояние между атомами хлора из разных молекул отражает межмолекулярное взаимодействие, т. е. ван-дер-ваальсову связь.
Островные структуры состоят из отдельных конечных группировок (часто молекул). В структуре кристаллического хлора, построенной из отдельных молекул Cl кратчайшее расстояние между двумя атомами Cl отвечает ковалентной связи, тогда как минимальное расстояние между атомами хлора из разных молекул отражает межмолекулярное взаимодействие, т. е. ван-дер-ваальсову связь.

 Цепочечные структуры могут состоять как из нейтральных, так и из валентно-насыщенных цепочек. Между атомами селена связь ковалентная, а между атомами из соседних цепочек ван-дер-ваальсова. В структуре. Na. HCO 3, водородные связи выстраивают карбонатные ионы (HCO 3)- в цепи, связь между которыми осуществляется через ионы Na+
Цепочечные структуры могут состоять как из нейтральных, так и из валентно-насыщенных цепочек. Между атомами селена связь ковалентная, а между атомами из соседних цепочек ван-дер-ваальсова. В структуре. Na. HCO 3, водородные связи выстраивают карбонатные ионы (HCO 3)- в цепи, связь между которыми осуществляется через ионы Na+

Рис. 17. Снежинки-скелетные кристаллы льда
Из опыта известно, что в кристаллическом веществе физические свойства одинаковы в параллельных направлениях, а представление о строении веществ требует, чтобы слагающие кристалл частицы (молекулы, атомы или ионы) находились одна от другой на некоторых конечных расстояниях. Исходя из этих предположений, возможно построить геометрическую схему строения кристаллического . Для этого положение каждой слагающей частицы можно отметить точкой. Вся кристаллическая постройка представится тогда системою точек, закономерно расположенных в пространстве, причем для любых параллельных направлений расстояния между точками будут одинаковыми. Такое правильное расположение точек в пространстве называют
пространственной решеткой, а если каждая точка представляет положение атома, иона или молекулы в кристалле - кристаллической решеткой.
Построение пространственной решетки можно себе представить следующим образом.
А 0 (рис. 18) обозначает центр атома или иона. Пусть ближайший к ней такой же центр обозначается точкой Ль тогда, на основании однородности кристаллического , на расстоянии А 1 А 2 = А 0 А 1 должен находиться центр А 2 ; продолжая это рассуждение далее, можно получить ряд точек: А 0 , А 1 , А 2 , А 3 …
Положим, что ближайшая точка к А 0 в другом направлении будетR 0 , тогда должна существовать частица S 0 на расстоянии R 0 S 0 = Л 0 R 0 и т. д., т. е. получится другой ряд одинаковых точекА 0 , R 0 , S 0 … Если через R 0 , S 0 и т. п. провести линии, параллельные A 0 , A 1 , A 2 , получатся одинаковые ряды R 0 , R 1 , R 2 , S 0 , S 1 , S 2 … и т. д

Рис. 18. Пространственная решетка
Врезультате сделанного построения получилась сетка, узлыкоторой соответствуют центрам частиц, слагающих кристалл.
Если представить себе, что в каждой точке В 0, Со и т. д. восстановлена такая же сетка, как и в A 0 , в результате этого построения получится пространственная решетка, которая в известном смысле и будет выражать геометрическое строение кристаллического .
Кристаллы это что
Теория пространственных решеток, созданная великим русским кристаллографом Е. С. Федоровым, получила блестящее подтверждение при исследовании структуры кристаллов посредством рентгеновских лучей. Эти исследования дают не только картины пространственных решеток, но и точные длины промежутков между частицами, находящимися в их узлах.

Рис. 19. Структура алмаза
При этом выяснилось, что существует несколько типов пространственных решеток, отличающихся как характером расположения частиц, так и химической природой их.
Отметим следующие типы пространственных решеток:
Атомные структурные решетки. В узлах этих решеток расположены атомы каких-либо веществ или элемента, соединяющиеся непосредственно между собою в кристаллическую решетку. Такого типа решетка характерна для алмаза, цинковой обманки и некоторых других минералов (см. рис. 19 и 20).
Ионные структурные решетки. В узлах этих решеток расположены ионы, т. е. атомы, имеющие положительный или отрицательный заряд.
Ионные решетки обычны для неорганических соединений, например галогенов щелочных металлов, силикатов и пр.
Прекрасным примером является решетка каменной соли (NaCl) (рис. 21). В ней ионы натрия (Na) по трем взаимно перпендикулярным направлениям чередуются с ионами хлора (Сl) через промежутки, равные 0,28 миллимикрона.

Рис. 20. Структура цинковой обманки
В кристаллических веществах с подобной структурой промежутки между атомами в молекуле равны промежуткам между молекулами, и само понятие молекулы теряет смысл для таких кристаллов. На рис. 20 каждый ион натрия имеет
сверху, снизу, справа, слева, спереди и сзади на равных от него расстояниях по одному иону хлора, которые принадлежат как к данной «молекуле», так и к соседним «молекулам», и нельзя сказать, с каким именно ионом хлора из этих шести составляет молекулу или составлял бы ее при переходе в газообразное состояние.
Кроме описанных выше типов, существуют молекулярные структурные решетки, в узлах которых находятся не атомы или ионы, а обособленные, электрически нейтральные молекулы. Молекулярные решетки особенно характерны для различных органических соединений или, например, для «сухого льда» - кристаллической СO 2 .

Рис. 21. Кристаллическая решетка каменной соли
Слабые («остаточные») связи между структурными единицами таких решеток обусловливают малую механическую прочность подобных решеток, их низкие температуры плавления и кипения. Существуют и такие кристаллы, в которых сочетаются различные типы решеток. В одних направлениях связи частиц являются ионными (валентными), а в других молекулярными (остаточными). Такое строение приводит к различной механической прочности в разных направлениях, обусловливая резкую анизотропию механических свойств. Так, кристаллы молибденита (MoS 2) легко раскалываются по направлению пинакоида (0001) и придают кристаллам этого минерала чешуйчатый облик, подобно кристаллам графита, где обнаруживается сходная структура. Причиной малой механической прочности в направлении перпендикулярном (0001) является отсутствие в этом направлении ионных связей. Целостность решетки здесь удерживается только связями молекулярного (остаточного) характера.
Принимая во внимание все изложенное выше, легко провести параллель между внутренней структурой аморфного вещества, с одной стороны, и кристаллического, с другой:
1.В аморфном веществе частицы располагаются в беспорядке, как бы закрепляя частично хаотическое состояние жидкости; поэтому некоторые исследователи называют , например , переохлажденными жидкостями.
2.В кристаллическом веществе частицы располагаются в стройном порядке и занимают определенное положение в узлах пространственной решетки.
Различие между кристаллическим и стекловатым (аморфным) веществом можно сравнить с тем различием, которое имеется между дисциплинированной воинской частью и рассеянной толпой. Естественно, что кристаллическое состояние более устойчиво, чем аморфное, и аморфное вещество будет легче растворяться, химически реагировать или плавиться. Природные всегда имеют тенденцию приобретать кристаллическое строение, «раскристаллизовываться», например (аморфный кремнезем) со временем переходит в халцедон - кристаллический кремнезем.
Вещество в кристаллическом состоянии обычно занимает несколько меньший объем, чем в аморфном виде, и имеет больший удельный вес; например альбит - полевой шпат состава NaAlSi 3 O 8 в аморфном состоянии занимает 10 куб. единиц, а в кристаллическом-только 9; 1 см 3 кристаллического кремнезема (кварца) весит 2,54 г, а такой же объем стекловатого кремнезема (сплавленного кварца) - только 2,22 г. Особый случай представляет лед, имеющий меньший удельный вес, чем , взятая в том же количестве.
ИССЛЕДОВАНИЕ КРИСТАЛЛОВ РЕНТГЕНОВСКИМИ ЛУЧАМИ
Вопрос о причинах закономерности в распределении физических свойств в кристаллическом веществе, вопрос о внутренней структуре кристаллов впервые пытался разрешить М. В. в 1749 г. на примере селитры. Этот вопрос затем был более широко разработан уже в конце XVIII в. французским кристаллографом Аюи. Аюи высказал предположение, что каждому веществу свойственна определенная кристаллическая форма. Это положение было в дальнейшем опровергнуто обнаружением явлений изоморфизма и полиморфизма. Указанные явления, играющие большую роль в минералогии, будут рассмотрены нами несколько позже.
Благодаря работам русского кристаллографа Е. С. Федорова и некоторых других кристаллографов, теория пространственных решеток, кратко изложенная в предыдущей главе, была разработана математически, и на основании исследования формы кристаллов были выведены возможные типы пространственных решеток; но только в XX в., благодаря исследованию кристаллов рентгеновскими лучами, эта теория была проверена на опыте и блестяще подтвердилась. Целому ряду физиков: Лауэ, Брэггам, Г. В. Вульфу и др. удалось, используя теорию пространственных решеток, доказать совершенно точно, что в узлах кристаллических решеток находятся в одних случаях атомы, а в других молекулы или ионы.
Открытые Рентгеном в 1895 г. лучи, носящие его имя, представляют один из видов лучистой энергии и по многим свойствам напоминают лучи света, отличаясь от них только длиной волны, которая в несколько тысяч раз меньше длины световых волн.

Рис. 22. Схема получения рентгенограммы кристалла по методу Лауэ:
А - рентгеновская трубка; В - диафрагма; С - кристалл; D - фотопластинка
В 1912 г. Лауэ воспользовался кристаллом, где атомы расположены по пространственной решетке, как дифракционной решеткой для получения интерференции рентгеновских лучей. В поставленном им исследовании узкий пучок параллельных рентгеновских лучей (рис. 22) пропускался через тонкий кристалл цинковой обманки С. На некотором расстоянии от кристалла и пер пендикулярно к пучку лучей была помещена фотографическая пластинка D, защищенная от непосредственного действия боковых рентгеновских лучей и от дневного света свинцовыми экранами.
При продолжительной выдержке в течение нескольких часов экспериментаторы получили картину, сходную с рис. 23.
Для световых лучей, обладающих сравнительно с размерами атомов большой длиной волны, атомные сетки пространственной решетки играют роль практически сплошных плоскостей, и световые лучи полностью отражаются от поверхности кристалла. Гораздо более короткие рентгеновские лучи, отраженные от многочисленных атомных сеток, расположенных на определенных расстояниях друг от друга, идя по одному и тому же направлению, будут интерферировать, то ослабляя, то усиливая друг друга. На фотографической пластинке, поставленной на их пути, усиленные лучи дадут при продолжительной экспозиции черные пятна, расположенные закономерно, в тесной связи с внутренним строением кристалла, т. е. с его атомной сеткой и с особенностями расположенных в ней отдельных атомов.
Если взять пластинку, вырезанную из кристалла в определенном кристаллографическом направлении, и произвести с ней тот жеопыт, то на рентгенограмме будет виден узор, соответствующий симметрии строения кристалла.
Более плотным атомным сеткам соответствуют наиболее темные пятна. Редко усаженные атомами грани дают слабые точки или почти не дают их. Центральное пятно на такой рентгенограмме получается от рентгеновских лучей, прошедших через пластинку

Рис. 23. Рентгенография кристалла каменной соли по оси 4-го порядка
по прямому пути; остальные пятна образуют лучи, отраженные от атомных сеток.
На рис. 23 изображена рентгенофотография кристалла каменной соли, из которого была вырезана пластинка около 3 мм толщиной, параллельная грани куба. Посредине видно большое пятно - след центрального пучка лучей.
Расположение мелких пятен симметрично и указывает на существование оси симметрии 4-го порядка и четырех плоскостей симметрии.
Вторая иллюстрация (рис. 24) изображает рентгенограмму кристалла кальцита. Снимок сделан в направлении оси симметрии 3-го порядка. Буквами О обозначены концы осей симметрии 2-го порядка.
В настоящее время для исследования структуры кристаллических тел пользуются разными методами. Существенной особенностью метода Лауэ, кратко описанного выше, является применение только крупных кристаллов, точно ориентированных по отношению к проходящему пучку рентгеновских лучей.
При невозможности пользоваться крупными кристаллами обычно применяется «метод порошков» (метод Дебая-Шерера). Громадное преимущество этого метода в том, что для него не требуется крупных кристаллов. Перед исследованием испытуемое вещество в тонко измельченном состоянии обычно спрессовывается в небольшой столбик. Этим методом можно исследовать не только спрессованные порошки, но и вести работу над готовыми образцами металлов в виде проволоки, если кристаллики их достаточно мелки.
При наличии большого количества кристаллов отражение может произойти от любой грани каждого кристалла. Поэтому на рентгенограмме, полученной по «методу порошков», обычно получается ряд линий, дающих характеристику исследуемого вещества.
Благодаря применению рентгеновских лучей для исследования кристаллов, наконец, была получена возможность проникнуть в область действительного расположения молекул, ионов и атомов внутри кристаллов и определить не только форму атомной решетки, но и расстояния между частицами, ее составляющими.
Изучение структуры кристаллов при помощи рентгеновских лучей позволило определить кажущиеся размеры ионов, входящих в состав данного кристалла. Метод определения величины радиуса иона или, как обычно говорят, ионного радиуса будет ясен из следующего примера. Исследование такого рода кристаллов как MgO, MgS и MgSe, с одной стороны, и MnO, MnS и MnSe, с другой, дало следующие межионные расстояния:
Для
MgO -2,10 Å МnО - 2,24 Å
MgS - 2,60 Å и MnS - 2,59 Å
MgSe - 2,73 Å MnSa - 2,73 Å,
где Å-обозначает величину „ангстрем», равную одной десятимиллионной миллиметра.
Сравнение приведенных величин показывает, что для межионного расстояния в соединениях MgO и МnО размеры ионов Mg и Мn Играют некоторую роль. В других же соединениях видно, что расстояния между ионами S и Se не зависит от входя щего в соединения другого иона, и ионы S и Se соприкасаются между собою, создавая плотнейшую упаковку ионов.

Рис. 24. Рентгенограмма кристалла кальцита на оси 3-го порядка
Вычисление дает для S -2 ионный радиус, равный 1,84 Å,
а для Se -2 - 1,93 Å. Зная ионные радиусы S -2 и Se -2 , можно вычислить и ионные радиусы других ионов. Так О 2 имеет ионный
радиус, равный 1,32Å. F -1 - 1,33Å, Na +l -0,98Å, Са+ 2 - 1,06,
К +1 - 1,33, Mg +2 -0,78Å, Аl +3 -0,57Å, Si +4 - 0,39Å и т. д. Величина ионного радиуса играет большую роль в вопросах изоморфизма и полиморфизма, что и будет рассмотрено в соответствующих разделах.
Рентгеноструктурное изучение минералов сильно продвинуло вперед современную минералогию, как в вопросах понимания строения минералов, так и связи их строения и состава с другими важными свойствами, как спайность, показатель преломления и др. Значение исследования минералов рентгеновскими лучами прекрасно выражается следующей фразой: «Если кристаллографы познавали минерал в той мере, в какой можно изучить здание, осматривая его снаружи, а химики пытались познать это здание, разрушив его и затем изучая в отдельности входившие в его состав материалы, то рентгеноструктурный анализ впервые позволил нам войти в здание и обозревать его внутреннее расположение и убранство».
Статья на тему Структура кристаллов
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Кристамллы (от греч. ксэуфбллпт, первоначально -- лёд, в дальнейшем -- горный хрусталь, кристалл) -- твёрдые тела, в которых атомырасположены закономерно, образуя трёхмерно-периодическую пространственную укладку -- кристаллическую решётку.
Кристаллы -- это твёрдые вещества, имеющие естественную внешнюю форму правильных симметричных многогранников, основанную на их внутренней структуре, то есть на одном из нескольких определённых регулярных расположений, составляющих вещество частиц (атомов, молекул, ионов).
Свойства:
Однородность. Это свойство проявляется в том, что два одинаковых элементарных объема кристаллического вещества, одинаково ориентированные в пространстве, но вырезанные в разных точках этого вещества, абсолютно одинаковы по всем своим свойствам: имеют один и тот же цвет, удельный вес, твердость, теплопроводность, электропроводность и др.
Необходимо иметь в виду, что реальные кристаллические вещества очень часто содержат постоянные примеси и включения, искажающие их кристаллические решетки. Поэтому абсолютной однородности в реальных кристаллах часто не бывает.
Анизотропия кристаллов
Многим кристаллам присуще свойство анизотропии, то есть зависимость их свойств от направления, тогда как в изотропных веществах (большинстве газов, жидкостей, аморфных твёрдых телах) или псевдоизотропных (поликристаллы) телах свойства от направлений не зависят. Процесс неупругого деформирования кристаллов всегда осуществляется по вполне определённым системам скольжения, то есть лишь по некоторым кристаллографическим плоскостям и лишь в некотором кристаллографическом направлении. В силу неоднородного и неодинакового развития деформации в различных участках кристаллической среды между этими участками возникает интенсивное взаимодействие через эволюцию полей микронапряжений.
В то же время существуют кристаллы, в которых анизотропия отсутствует.
В физике мартенситной неупругости накоплен богатый экспериментальный материал, особенно по вопросам эффектов памяти формы и пластичности превращения. Экспериментально доказано важнейшее положение кристаллофизики о преимущественном развитии неупругих деформаций почти исключительно посредством мартенситных реакций. Но принципы построения физической теории мартенситной неупругости неясны. Аналогичная ситуация имеет место в случае деформации кристаллов механическим двойникованием.
Значительные успехи достигнуты в изучении дислокационной пластичности металлов. Здесь не только понятны основные структурно-физические механизмы реализации процессов неупругой деформации, но и созданы эффективные способы расчёта явлений.
Способнось самоотгоняться - свойство кристаллов образовывать грани при свободном росте.Так. если выточенный из какого-либо вещества шарик, например поваренная соль, поместить в ее пересыщенный раствор, то через некоторе время этот шарик примет форму куба. В противоположенность этому стеклянный шарик не изменит свою форму так как аморфное вещество не может самоотгоняться.
Постоянная точка плавления. Если нагревать кристаллическое тело, то температура его будет повышаться до определенного предела, при дальнейшем нагревании вещество начнет плавиться, а температура некоторре время останется постоянной, так как все тепло пойдет на разрушение кристаллической решетки. Температура, при которой начинается плавленеиЮ называется температурой плавления.
Систематика кристаллов
Кристаллическая структура
Кристаллическая структура, будучи индивидуальной для каждого вещества, относится к основным физико-химическим свойствам этого вещества. Кристаллимческая структумра -- такая совокупность атомов, в которой с каждой точкой кристаллической решётки связана определённая группа атомов, называемая мотивной единицей, причем все такие группы одинаковые по составу, строению и ориентации относительно решётки. Можно считать, что структура возникает в результате синтеза решётки и мотивной единицы, в результате размножения мотивной единицы группой трансляции.
В простейшем случае мотивная единица состоит из одного атома, например в кристаллах меди или железа. Возникающая на основе такой мотивной единицы структура геометрически весьма сходна с решёткой, но все же отличается тем, что составлена атомами, а не точками. Часто это обстоятельство не учитывают, и термины «кристаллическая решётка» и «кристаллическая структура» для таких кристаллов употребляются как синонимы, что нестрого. В тех случаях, когда мотивная единица более сложна по составу -- состоит из двух или большего числа атомов, геометрического сходства решётки и структуры нет, и смещение этих понятий приводит к ошибкам. Так, например, структура магния или алмаза не совпадает геометрически с решёткой: в этих структурах мотивные единицы состоят из двух атомов.
Основными параметрами, характеризующими кристаллическую структуру, некоторые из которых взаимосвязаны, являются следующие:
§ тип кристаллической решётки (сингония, решётка Браве);
§ число формульных единиц, приходящихся на элементарную ячейку;
§ пространственная группа;
§ параметры элементарной ячейки (линейные размеры и углы);
§ координаты атомов в ячейке;
§ координационные числа всех атомов.
Структурный тип
Кристаллические структуры, обладающие одинаковой пространственной группой и одинаковым размещением атомов по кристаллохимическим позициям (орбитам), объединяют в структурные типы.
Наиболее известны структурные типы меди, магния, б-железа, алмаза (простые вещества), хлорида натрия, сфалерита, вюрцита, хлорида цезия, флюорита (бинарные соединения),перовскита, шпинели (тройные соединения).
Кристаллическая решётка
Составляющие данное твёрдое вещество частицы образуют кристаллическую решётку. Если кристаллические решётки стереометрически (пространственно) одинаковы или сходны (имеют одинаковую симметрию), то геометрическое различие между ними заключается, в частности, в разных расстояниях между частицами, занимающими узлы решётки. Сами расстояния между частицами называются параметрами решётки. Параметры решётки, а также углы геометрических многогранников определяются физическими методами структурного анализа, например, методами рентгеновского структурного анализа.
Размещено на http://www.allbest.ru/
Рис. Кристаллическая решетка
Часто твёрдые вещества образуют (в зависимости от условий) более чем одну форму кристаллической решётки; такие формы называются полиморфными модификациями. Например, среди простых веществ известны ромбическая и моноклинная сера, графит и алмаз, которые являются гексагональной и кубической модификациями углерода, среди сложных веществ -- кварц, тридимит и кристобалит представляют собой различные модификации диоксида кремния.
Виды кристаллов
Следует разделить идеальный и реальный кристалл.
Идеальный кристалл
Является, по сути, математическим объектом, имеющим полную, свойственную ему симметрию, идеализированно ровные гладкие грани.
Реальный кристалл
Всегда содержит различные дефекты внутренней структуры решетки, искажения и неровности на гранях и имеет пониженную симметрию многогранника вследствие специфики условий роста, неоднородности питающей среды, повреждений и деформаций. Реальный кристалл не обязательно обладает кристаллографическими гранями и правильной формой, но у него сохраняется главное свойство -- закономерное положение атомов в кристаллической решётке.
Дефекты кристаллической решетки (реальное строение кристаллов)
В реальных кристаллах всегда имеются отклонения от идеального порядка в расположении атомов, называемые несовершенствами или дефектами решетки. По геометрии вызываемых ими нарушений решетки дефекты подразделяют на точечные, линейные и поверхностные.
Точечные дефекты
На рис. 1.2.5 показаны различные виды точечных дефектов. Это вакансии - пустые узлы решетки, «свои» атомы в междоузлии и атомы примесей в узлах решетки и междоузлиях. Основная причина образования первых двух видов дефектов - движение атомов, интенсивность которого возрастает с повышением температуры.
Рис. 1.2.5. Типы точечных дефектов кристаллической решетки: 1 - вакансия, 2 - атом в междоузлии, 3 и 4 - атомы примесей в узле и междоузлии соответственно
Вокруг любого точечного дефекта возникает местное искажение решетки радиусом R в 1…2 периода решетки (см. рис. 1.2.6), поэтому, если таких дефектов много, они влияют на характер распределения межатомных сил связи и, соответственно, на свойства кристаллов.
Рис. 1.2.6. Локальное искажение кристаллической решетки вокруг вакансии (а) и примесного атома в узле решетки (б)
Линейные дефекты
Линейные дефекты называются дислокациями. Их появление вызвано наличием в отдельных частях кристалла «лишних» атомных полуплоскостей (экстраплоскости). Они возникают в процессе кристаллизации металлов (из-за нарушения порядка заполнения атомных слоев) или в результате их пластического деформирования, как показано на рис. 1.2.7.
Рис. 1.2.7. Образование краевой дислокации () в результате частичного сдвига верхней части кристалла под действием усилия: АВСD - плоскость скольжения; EFGН - экстраплоскость; EН - линия краевой дислокации
Видно, что под влиянием сдвигающего усилия произошел частичный сдвиг верхней части кристалла вдоль некоторой плоскости скольжения («легкого сдвига») АВСD. В результате образовалась экстраплоскость EFGH. Поскольку она не имеет продолжения вниз, вокруг ее края EH возникает упругое искажение решетки радиусом в несколько межатомных расстояний (т.е. 10 -7 см - см. тема 1.2.1), протяженность же этого искажения во много раз больше (может доходить до 0,1…1 см).
Такое несовершенство кристалла вокруг края экстраплоскости является линейным дефектом решетки и называется краевой дислокацией.
Важнейшие механические свойства металлов - прочность и пластичность (см. тема 1.1) - определяются наличием дислокаций и их поведением при нагружении тела.
Остановимся на двух особенностях механизма перемещения дислокаций.
1. Дислокации могут весьма легко (при малой нагрузке) передвигаться вдоль плоскости скольжения посредством «эстафетного» перемещения экстраплоскости. На рис. 1.2.8 показан начальный этап такого движения (двумерный рисунок в плоскости, перпендикулярной линии краевой дислокации).
Рис. 1.2.8. Начальный этап эстафетного перемещения краевой дислокации (). А-А - плоскость скольжения, 1-1 экстраплоскость (исходная позиция)
Под действием усилия атомы экстраплоскости (1-1) отрывают от плоскости (2-3) атомы (2-2), расположенные выше плоскости скольжения. В результате эти атомы образуют новую экстраплоскость (2-2); атомы «старой» экстраплоскости (1-1) занимают освободившиеся места, достраивая плоскость (1-1-3). Этот акт означает исчезновение «старой» дислокации, связанной с экстраплоскостью (1-1), и возникновение «новой», связанной с экстраплоскостью (2-2), или, другими словами, передачу «эстафетной палочки» - дислокации на одно межплоскостное расстояние. Такое эстафетное перемещение дислокации будет продолжаться до тех пор, пока она не дойдет до края кристалла, что будет означать сдвиг его верхней части на одно межплоскостное расстояние (т.е. пластическую деформацию).
Этот механизм не требует больших усилий, т.к. состоит из последовательных микросмещений, затрагивающих лишь ограниченное число атомов, окружающих экстраплоскость.
2. Очевидно, однако, что такая легкость скольжения дислокаций будет наблюдаться лишь в том случае, когда на их пути отсутствуют какие - либо препятствия. Такими препятствиями являются любые дефекты решетки (особенно линейные и поверхностные!), а также частицы других фаз, если они присутствуют в материале. Эти препятствия создают искажения решетки, преодоление которых требует дополнительных внешних усилий, поэтому могут заблокировать движение дислокаций, т.е. сделать их неподвижными.
Поверхностные дефекты
Все промышленные металлы (сплавы) являются поликристаллическими материалами, т.е. состоят из огромного количества мелких (обычно 10 -2 …10 -3 см), хаотически ориентированных кристалликов, называемых зернами. Очевидно, что периодичность решетки, присущая каждому зерну (монокристаллу), в таком материале нарушена, поскольку кристаллографические плоскости зерен повернуты относительно друг друга на угол б (см. рис. 1.2.9), величина которого колеблется от долей до нескольких десятков градусов.
Рис. 1.2.9. Схема строения границ зерен в поликристаллическом материале
Граница между зернами представляет собой переходный слой шириной до 10 межатомных расстояний, обычно с неупорядоченным расположением атомов. Это место скопления дислокаций, вакансий, примесных атомов. Поэтому в объеме поликристаллического материала границы зерен являются двумерными, поверхностными дефектами.
Влияние дефектов решетки на механические свойства кристаллов. Пути повышения прочности металлов.
Прочность - это способность материала сопротивляться деформации и разрушению под действием внешней нагрузки.
Под прочностью кристаллических тел понимают их сопротивление приложенной нагрузке, стремящейся сдвинуть или, в пределе, оторвать одну часть кристалла относительно другой.
Наличие в металлах подвижных дислокаций (уже в процессе кристаллизации возникает до 10 6 …10 8 дислокаций в сечении, равном 1см 2) приводит к их пониженной сопротивляемости нагружению, т.е. высокой пластичности и невысокой прочности.
Очевидно, что наиболее эффективным способом повышения прочности будет удаление дислокаций из металла. Однако такой путь не технологичен, т.к. бездислокационные металлы удается получать лишь в виде тонких нитей (так называемых «усов») диаметром в несколько микрон и длиной до 10 мкм.
Поэтому практические способы упрочнения основаны на торможении, блокировании подвижных дислокаций путем резкого увеличения числа дефектов решетки (в первую очередь линейных и поверхностных!), а также создании многофазных материалов
Такими традиционными методами повышения прочности металлов являются:
– пластическое деформирование (явление наклепа или нагартовки),
– термическая (и химико-термическая) обработка,
– легирование (введение специальных примесей) и, наиболее общий подход, - это создание сплавов.
В заключение следует отметить, что повышение прочности, основанное на блокировании подвижных дислокаций, приводит к снижению пластичности и ударной вязкости и, соответственно, эксплуатационной надежности материала.
Поэтому вопрос о степени упрочнения необходимо решать индивидуально, исходя из назначения и условий работы изделия.
Полиморфизм в буквальном смысле слова означает многоформенность, т.е. явление, когда одинаковые по химическому составу вещества кристаллизуются в различных структурах и образуют кристаллы различных сингогий. Например алмаз и графит имеют одинаковый химический состав, но различные структуры, оба минерала резко отличаются по физ. свойствам. Другим примером может служить кальцит и арагонит - они имеют одинаковый состав СаСО 3 , но представляют различные полиморфные модификации.
Явление полиморфизма связаны с условиями образования кристаллических веществ и обусловлены тем, что в различных термодинамических условиях устойчивыми являются только определенные структуры. Так, металлические олово (так называемое белое олово) при понижении температуры ниже -18 С 0 становится неустойчивым и рассыпается образуя «серое олово» уже иной структуры
Изоморфизм. Сплавы металлов представляют собой кристаллические структуры переменного состава, в которых атомы одного элемента располагаются в промежутках кристаллической решетки другого. Это так называемые твердые растворы второго рода.
В отличие от твердых растворов второго рода в твердых растворах первого рода атомы или ионы одного кристаллического вещества могут замещаться атомами или ионами другого. Последние располагаются в узлах кристаллической решетки. Подобного рода растворы называются изоморфными смесями.
Условия необходимые для проявления изоморфизма:
1) Замещаться могут только ионы одного знака, т.е., катион на катион, а анион на анион
2) Замещаться могут только атомы или ионы близкого размера, т.е. разница величины ионных радиусов не должна превышать при совершенном изоморфизме 15% и несовершенном 25% (например Са 2+ на Mg 2+)
3) Замещаться могут только ионы, близкие по степени поляризации (т.е. по степени ионности-ковалентности связи)
4) Замещаться могут только элементы, имеющие одинаковое координационное число в данной кристаллической структуре
5) изоморфные замещения должны происходить таким образом. Чтобы не нарушался электростатический баланс кристаллической решетки.
6) изоморфные замещения протекают в сторону приращения энергии решетки.
Типы изоморфизма. Различают 4 типа изоморфизма:
1) изовалентный изоморфизм характеризуется тем, что в этом случае происходит ионов одинаковой валентности причем разница в размерах ионных радиусов не должна быть более 15%
2) гетеровалентный изоморфизм. При этом происходит замещение ионов различной валентности. При таком замещении один ион не может замещаться другим без того, чтобы нарушился электростатический баланс кристаллической решетки, поэтому при гетеровалентном изоморфизме замещается не ион, как при гетеровалентном, а группа ионов определенной валентности на другую группу ионов при сохранении той же суммарной валентности.
Необходимо в этом случае всегда помнить что замещение иона одной валентности на ион другой всегда связано с компенсацией валентности. Эта компенсация может происходить как в катионной, так и в анионной части соединений. При этом необходимо соблюдение следующих условий:
А) сумма валентностей замещаемых ионов должна быть равна сумме валентностей замещающих ионов.
Б) сумма ионных радиусов замещаемых ионов должна быть близка к сумме ионных радиусов замещающих ионов и может отличаться от нее не более чем на 15% (для совершенного изоморфизма)
3) изоструктурный. Происходит замещение не одного иона на другой или группы ионов на другую группу, а замещение целого «блока» одной кристаллической решетки на другой такой же «блок». Это может происходить только в том случае, если структуры минералов однотипны и имеют близкие размеры элементарных ячеек.
4) изоморфизм особого рода.
кристалл решётка дефект дислокация
Размещено на Allbest.ru
Подобные документы
Характеристика пьезоэлектрического эффекта. Изучение кристаллической структуры эффекта: модельное рассмотрение, деформации кристаллов. Физический механизм обратного пьезоэлектрического эффекта. Свойства пьезоэлектрических кристаллов. Применение эффекта.
курсовая работа , добавлен 09.12.2010
Сведения о колебаниях кристаллических решёток, функции, описывающие их физические величины. Кристаллографические системы координат. Расчет энергии взаимодействия атомов в ковалентных кристаллах, спектра колебаний кристаллической решётки вольфромата бария.
дипломная работа , добавлен 09.01.2014
Прохождение тока через электролиты. Физическая природа электропроводности. Влияние примесей, дефектов кристаллической структуры на удельное сопротивление металлов. Cопротивление тонких металлических пленок. Контактные явления и термоэлектродвижущая сила.
реферат , добавлен 29.08.2010
Понятие и классификация дефектов в кристаллах: энергетические, электронные и атомные. Основные несовершенства кристаллов, образование точечных дефекто, их концентрация и скорость перемещения по кристаллу. Диффузия частиц за счет движений вакансий.
реферат , добавлен 19.01.2011
Сущность полиморфизма, история его открытия. Физические и химические свойства полиморфных модификаций углерода: алмаза и графита, их сравнительный анализ. Полиморфные превращения жидких кристаллов, тонких пленок дийодида олова, металлов и сплавов.
курсовая работа , добавлен 12.04.2012
Кристаллическое и аморфное состояния твердых тел, причины точечных и линейных дефектов. Зарождение и рост кристаллов. Искусственное получение драгоценных камней, твердые растворы и жидкие кристаллы. Оптические свойства холестерических жидких кристаллов.
реферат , добавлен 26.04.2010
История развития представления о жидких кристаллах. Жидкие кристаллы, их виды и основные свойства. Оптическая активность жидких кристаллов и их структурные свойства. Эффект Фредерикса. Физический принцип действия устройств на ЖК. Оптический микрофон.
учебное пособие , добавлен 14.12.2010
Кристаллизация как процесс перехода металла из жидкого состояния в твердое с образованием кристаллической структуры. Схема образования шва при дуговой сварке. Ключевые факторы и условия, необходимые для начала роста кристаллов из жидкого металла.
презентация , добавлен 26.04.2015
Изучение структуры (образование кристаллитами, расположенными хаотическим образом) и способов получения (охлаждение расплава, напыление из газовой фазы, бомбардировка кристаллов нейронами) стекол. Ознакомление с процессами кристаллизации и стеклования.
реферат , добавлен 18.05.2010
Дефекты реальных кристаллов, принцип работы биполярных транзисторов. Искажение кристаллической решетки в твердых растворах внедрения и замещения. Поверхностные явления в полупроводниках. Параметры транзистора и коэффициент передачи тока эмиттера.
Содержание статьи
КРИСТАЛЛЫ – вещества, в которых мельчайшие частицы (атомы, ионы или молекулы) «упакованы» в определенном порядке. В результате при росте кристаллов на их поверхности самопроизвольно возникают плоские грани, а сами кристаллы принимают разнообразную геометрическую форму. Каждый, кто побывал в музее минералогии или на выставке минералов, не мог не восхититься изяществом и красотой форм, которые принимают «неживые» вещества.
А кто не любовался снежинками, разнообразие которых поистине бесконечно! Еще в 17 в. знаменитый астроном Иоганн Кеплер написал трактат О шестиугольных снежинках, а спустя три столетия были изданы альбомы, в которых представлены коллекции увеличенных фотографий тысяч снежинок, причем ни одна из них не повторяет другую.
Интересно происхождения слова «кристалл» (оно звучит почти одинаково во всех европейских языках). Много веков назад среди вечных снегов в Альпах, на территории современной Швейцарии, нашли очень красивые, совершенно бесцветные кристаллы, очень напоминающие чистый лед. Древние натуралисты так их и назвали – «кристаллос», по-гречески – лед; это слово происходит от греческого «криос» – холод, мороз. Полагали, что лед, находясь длительное время в горах, на сильном морозе, окаменевает и теряет способность таять. Один из самых авторитетных античных философов Аристотель писал, что «кристаллос рождается из воды, когда она полностью утрачивает теплоту». Римский поэт Клавдиан в 390 то же самое описал стихами:
Ярой альпийской зимой лед превращается в камень.
Солнце не в силах затем камень такой растопить .
Аналогичный вывод сделали в древности в Китае и Японии – лед и горный хрусталь обозначали там одним и тем же словом. И даже в 19 в. поэты нередко соединяли воедино эти образы:
Едва прозрачный лед, над озером тускнея,
Кристаллом покрывал недвижные струи.
А.С.Пушкин. К Овидию
Особое место среди кристаллов занимают драгоценные камни, которые с древнейших времен привлекают внимание человека. Люди научились получать искусственно очень многие драгоценные камни. Например, подшипники для часов и других точных приборов уже давно делают из искусственных рубинов. Получают искусственно и прекрасные кристаллы, которые в природе вообще не существуют. Например, фианиты – их название происходит от сокращения ФИАН – Физический институт Академии наук, где они впервые были получены. Фианиты – кристаллы кубического оксида циркония ZrO 2 , которые внешне очень похожи на бриллианты.
Строение кристаллов.
В зависимости от строения, кристаллы делятся на ионные, ковалентные, молекулярные и металлические. Ионные кристаллы построены из чередующихся катионов и анионов, которые удерживаются в определенном порядке силами электростатического притяжения и отталкивания. Электростатические силы ненаправленные: каждый ион может удержать вокруг себя столько ионов противоположного знака, сколько помещается. Но при этом силы притяжения и отталкивания должны быть уравновешены и должна сохраняться общая электронейтральность кристалла. Все это с учетом размеров ионов приводит к различным кристаллическим структурам. Так, при взаимодействии ионов Na + (их радиус 0,1 нм) и Cl – (радиус 0,18 нм) возникает октаэдрическая координация: каждый ион удерживает около себя шесть ионов противоположного знака, расположенных по вершинам октаэдра. При этом все катионы и анионы образуют простейшую кубическую кристаллическую решетку, в которой вершины куба попеременно заняты ионами Na + и Cl – . Аналогично устроены кристаллы KCl, BaO, CaO, ряда других веществ.
Ионы Cs + (радиус 0,165 нм) по размерам близки ионам Cl – , и возникает кубическая координация: каждый ион окружен восемью ионами противоположного знака, расположенными в вершинах куба. При этом образуется объемноцентрированная кристаллическая решетка: в центре каждого куба, образованного восемью катионами, расположен один анион, и наоборот. (Интересно, что при 445° С CsCl переходит в простую кубическую решетку типа NaCl.) Более сложно устроены кристаллические решетки CaF 2 (флюорита), многих других ионных соединений. В некоторых ионных кристаллах сложные многоатомные анионы могут соединяться в цепи, слои или образовывать трехмерный каркас, в полостях которого располагаются катионы. Так, например, устроены силикаты. Ионные кристаллы образуют большинство солей неорганических и органических кислот, оксиды, гидроксиды, соли. В ионных кристаллах связи между ионами прочные, поэтому такие кристаллы имеют высокие температуры плавления (801° С для NaCl, 2627° С для СаО).
В ковалентных кристаллах (их еще называют атомными) в узлах кристаллической решетки находятся атомы, одинаковые или разные, которые связаны ковалентными связями. Эти связи прочные и направлены под определенными углами. Типичным примером является алмаз; в его кристалле каждый атом углерода связан с четырьмя другими атомами, находящимися в вершинах тетраэдра. Ковалентные кристаллы образуют бор, кремний, германий, мышьяк, ZnS, SiO 2 , ReO 3 , TiO 2 , CuNCS. Поскольку между полярной ковалентной и ионной связью нет резкой границы, то же справедливо и для ионных и ковалентных кристаллов. Так, заряд на атоме алюминия в Al 2 O 3 равен не +3, а лишь +0,4, что свидетельствует о большом вкладе ковалентной структуры. В то же время в алюминате кобальта CoAl 2 O 4 заряд на атомах алюминия увеличивается до +2,8, что означает преобладание ионных сил. Ковалентные кристаллы, как правило, твердые и тугоплавкие.
Молекулярные кристаллы построены из изолированных молекул, между которыми действуют сравнительно слабые силы притяжения. В результате такие кристаллы имеют намного меньшие температуры плавления и кипения, твердость их низка. Так, кристаллы благородных газов (они построены из изолированных атомов) плавятся уже при очень низких температурах. Из неорганических соединений молекулярные кристаллы образуют многие неметаллы (благородные газы, водород, азот, белый фосфор, кислород, сера, галогены), соединения, молекулы которых образованы только ковалентными связями (H 2 O, HCl, NH 3 , CO 2 и др.). Этот тип кристаллов характерен также почти для всех органических соединений. Прочность молекулярных кристаллов зависит от размеров и сложности молекул. Так, кристаллы гелия (радиус атома 0,12 нм) плавятся при –271,4°С (под давлением 30 атм), а ксенона (радиус 0,22 нм) – при –111,8° С; кристаллы фтора плавятся при –219,6° С, а иода – при +113,6° С; метана СН 4 – при –182,5° С, а триаконтана С 30 Н 62 – при +65,8° С.
Металлические кристаллы образуют чистые металлы и их сплавы. Такие кристаллы можно увидеть на изломе металлов, а также на поверхности оцинкованной жести. Кристаллическая решетка металлов образована катионами, которые связаны подвижными электронами («электронным газом»). Такое строение обусловливает электропроводность, ковкость, высокую отражательную способность (блеск) кристаллов. Структура металлических кристаллов образуется в результате разной упаковки атомов-шаров. Щелочные металлы, хром, молибден, вольфрам и др. образуют объемноцентрированную кубическую решетку; медь, серебро, золото, алюминий, никель и др. – гранецентрированную кубическую решетку (в ней помимо 8 атомов в вершинах куба имеются еще 6, расположенные в центре граней); бериллий, магний, кальций, цинк и др. – так называемую гексагональную плотную решетку (в ней 12 атомов расположены в вершинах прямоугольной шестигранной призмы, 2 атома – в центре двух оснований призмы и еще 3 атома – в вершинах треугольника в центре призмы).
Все кристаллические соединения можно разделить на моно- и поликристаллические. Монокристалл представляет собой монолит с единой ненарушенной кристаллической решеткой. Природные монокристаллы больших размеров встречаются очень редко. Большинство кристаллических тел являются поликристаллическими, то есть состоят из множества мелких кристалликов, иногда видных только при сильном увеличении.
Рост кристаллов.
Многие видные ученые, внесшие большой вклад в развитие химии, минералогии, других наук, начинали свои первые опыты именно с выращивания кристаллов. Помимо чисто внешних эффектов, эти опыты заставляют задумываться на тем, как устроены кристаллы и как они образуются, почему разные вещества дают кристаллы разной формы, а некоторые вовсе не образуют кристаллов, что надо сделать, чтобы кристаллы получились большими и красивыми.
Вот простая модель, поясняющая суть кристаллизации. Представим, что в большом зале укладывают паркет. Легче всего работать с плитками квадратной формы – как ни поверни такую плитку, она все равно подойдет к своему месту, и работа пойдет быстро. Именно поэтому легко кристаллизуются соединения, состоящие из атомов (металлы, благородные газы) или небольших симметричных молекул. Такие соединения, как правило, не образуют некристаллических (аморфных) веществ.
Труднее выложить паркет из прямоугольных дощечек, особенно если у них с боков имеются пазы и выступы – тогда каждую дощечку можно уложить на свое место одним единственным способом. Особенно трудно выложить паркетный узор из дощечек сложной формы.
Если паркетчик очень торопится, то плитки будут поступать к месту укладки слишком быстро. Понятно, что правильного узора теперь не получится: если хотя бы в одном месте плитку перекосит, то дальше все пойдет криво, появятся пустоты (как в старой компьютерной игре «Тетрис», в которой «стакан» заполняется деталями слишком быстро). Ничего хорошего не получится и в том случае, если в большом зале начнут укладывать паркет сразу десяток мастеров – каждый со своего места. Даже если они будут работать не спеша, крайне сомнительно, чтобы соседние участки оказались хорошо состыкованными, и в целом, вид у помещения получится весьма неприглядным: в разных местах плитки расположены в разном направлении, а между отдельными участками ровного паркета зияют дыры.
Примерно те же процессы происходят и при росте кристаллов, только сложность здесь еще и в том, что частички должны укладываться не в плоскости, а в объеме. Но ведь никакого «паркетчика» здесь нет – кто же укладывает частички вещества на свое место? Оказывается, они укладываются сами, потому что непрерывно совершают тепловые движения и «ищут» самое подходящее для себя место, где им будет наиболее «удобно». В данном случае «удобство» подразумевает также и наиболее энергетически выгодное расположение. Попав на такое место на поверхности растущего кристалла, частица вещества может там остаться и через некоторое время оказаться уже внутри кристалла, под новыми наросшими слоями вещества. Но возможно и другое – частица вновь уйдет с поверхности в раствор и снова начнет «искать», где ей удобнее устроиться.
Каждое кристаллическое вещество имеет определенную свойственную ему внешнюю форму кристалла. Например, для хлорида натрия эта форма – куб, для алюмокалиевых квасцов – октаэдр. И даже если сначала такой кристалл имел неправильную форму, он все равно рано или поздно превратится в куб или октаэдр. Более того, если кристалл с правильной формой специально испортить, например, отбить у него вершины, повредить ребра и грани, то при дальнейшем росте такой кристалл начнет самостоятельно «залечивать» свои повреждения. Происходит это потому, что «правильные» грани кристалла растут быстрее, «неправильные» – медленнее. Чтобы убедиться в этом, был проведен такой опыт: из кристалла поваренной соли выточили шар, а потом поместили его в насыщенный раствор NaCl; через некоторое время шар сам постепенно превратился в куб! Рис. 6 Формы кристаллов некоторых минералов
Если процесс кристаллизации идет не слишком быстро, а частицы обладают удобной для укладки формой и высокой подвижностью, они легко находят свое место. Если же резко снизить подвижность частиц с низкой симметрией, то они «застывают» как попало, образуя прозрачную массу, похожую на стекло. Такое состояние вещества так и называют – стеклообразным. Примером может служить обычное оконное стекло. Если стекло долго держать сильно нагретым, когда частицы в нем достаточно подвижны, в нем начнут расти кристаллы силикатов. Такое стекло теряет прозрачность. Стеклообразными могут быть не только силикаты. Так, при медленном охлаждении этилового спирта он кристаллизуется при температуре –113,3° С, образуя белую снегообразную массу. Но если охлаждение вести очень быстро (опустить тонкую ампулу со спиртом в жидкий азот с температурой –196° С), спирт застынет так быстро, что его молекулы не успеют построить правильный кристалл. В результате получится прозрачное стекло. То же происходит и с силикатным стеклом (например, оконным). При очень быстром охлаждении (миллионы градусов в секунду) даже металлы можно получить в некристаллическом стеклообразном состоянии.
Трудно кристаллизуются вещества с «неудобной» формой молекул. К таким веществам относятся, например, белки и другие биополимеры. Но и обычный глицерин, который имеет температуру плавления +18° С, при охлаждении легко переохлаждается, постепенно застывая в стеклообразную массу. Дело в том, что уже при комнатной температуре глицерин очень вязкий, а при охлаждении становится совсем густым. При этом несимметричным молекулам глицерина очень трудно выстроиться в строгом порядке и образовать кристаллическую решетку.
Способы выращивания кристаллов.
Кристаллизацию можно вести разными способами. Один из них – охлаждение насыщенного горячего раствора. При каждой температуре в данном количестве растворителя (например, в воде) может раствориться не более определенного количества вещества. Например, в 100 г воды при 90° С может раствориться 200 г алюмокалиевых квасцов. Такой раствор называется насыщенным. Будем теперь охлаждать раствор. С понижением температуры растворимость большинства веществ уменьшается. Так, при 80° С в 100 г воды можно растворить уже не более 130 г квасцов. Куда же денутся остальные 70 г? Если охлаждение вести быстро, избыток вещество просто выпадет в осадок. Если этот осадок высушить и рассмотреть в сильную лупу, то можно увидеть множество мелких кристалликов.
При охлаждении раствора частички вещества (молекулы, ионы), которые уже не могут находиться в растворенном состоянии, слипаются друг с другом, образуя крошечные кристаллы-зародыши. Образованию зародышей способствуют примеси в растворе, например пыль, мельчайшие неровности на стенках сосуда (химики иногда специально трут стеклянной палочкой по внутренним стенкам стакана, чтобы помочь кристаллизации вещества). Если раствор охлаждать медленно, зародышей образуется немного, и, обрастая постепенно со всех сторон, они превращаются в красивые кристаллики правильной формы. При быстром же охлаждении образуется много зародышей, причем частички из раствора будут «сыпаться» на поверхность растущих кристалликов, как горох из порванного мешка; конечно, правильных кристаллов при этом не получится, потому что находящиеся в растворе частицы могут просто не успеть «устроиться» на поверхности кристалла на положенное им место. Кроме того, множество быстро растущих кристалликов так же мешают друг другу, как несколько паркетчиков, работающих в одной комнате. Посторонние твердые примеси в растворе также могут играть роль центров кристаллизации, поэтому чем чище раствор, тем больше шансов, что центров кристаллизации будет немного.
Охладив насыщенный при 90° С раствор квасцов до комнатной температуры, мы получим в осадке уже 190 г, потому что при 20° С в 100 г воды растворяется только 10 г квасцов. Получится ли при этом один большой кристалл правильной формы массой 190 г? К сожалению, нет: даже в очень чистом растворе вряд ли начнет расти один-единственный кристалл: масса кристалликов может образоваться на поверхности остывающего раствора, где температура немного ниже, чем в объеме, а также на стенках и дне сосуда.
Метод выращивания кристаллов путем постепенного охлаждения насыщенного раствора неприменим к веществам, растворимость которых мало зависит от температуры. К таким веществам относятся, например, хлориды натрия и алюминия, ацетат кальция.
Другой метод получения кристаллов – постепенное удаление воды из насыщенного раствора. «Лишнее» вещество при этом кристаллизуется. И в этом случае чем медленнее испаряется вода, тем лучше получаются кристаллы.
Третий способ – выращивание кристаллов из расплавленных веществ при медленном охлаждении жидкости. При использовании всех способов наилучшие результаты получаются, если используется затравка – небольшой кристалл правильной формы, который помещают в раствор или расплав. Таким способом получают, например, кристаллы рубина. Выращивание кристаллов драгоценных камней проводят очень медленно, иногда годами. Если же ускорить кристаллизацию, то вместо одного кристалла получится масса мелких.
Кристаллы могут также расти при конденсации паров – так получаются снежинки и узоры на холодном стекле. При вытеснении металлов из растворов их солей с помощью более активных металлов также образуются кристаллы. Например, если в раствор медного купороса опустить железный гвоздь, он покроется красным слоем меди. Но образовавшиеся кристаллы меди настолько мелкие, что их можно разглядеть только под микроскопом. На поверхности гвоздя медь выделяется очень быстро, поэтому и кристаллы ее слишком мелкие. Но если процесс замедлить, кристаллы получатся большими. Для этого медный купорос надо засыпать толстым слоем поваренной соли, положить на него кружок фильтровальной бумаги, а сверху – железную пластинку диаметром чуть поменьше. Осталось налить в сосуд насыщенный раствор поваренной соли. Медный купорос начнет медленно растворяться в рассоле (растворимость в нем меньше, чем в чистой воде). Ионы меди (в виде комплексных анионов CuCl 4 2– зеленого цвета) будут очень медленно, в течение многих дней, диффундировать вверх; за процессом можно наблюдать по движению окрашенной границы.
Достигнув железной пластинки, ионы меди восстанавливаются до нейтральных атомов. Но так как процесс этот происходит очень медленно, атомы меди выстраиваются в красивые блестящие кристаллы металлической меди. Иногда эти кристаллы образуют разветвления – дендриты. Меняя условия опыта (температура, размер кристаллов купороса, толщина слоя соли и т.п.), можно менять условия кристаллизации меди.
Переохлажденные растворы.
Иногда насыщенный раствор при охлаждении не кристаллизуется. Такой раствор, который содержит в определенном количестве растворителя больше растворенного вещества, чем это «положено» при данной температуре, называется пересыщенным раствором. Пересыщенный раствор невозможно получить даже очень длительным перемешиванием кристаллов с растворителем, он может образоваться только путем охлаждения горячего насыщенного раствора. Поэтому такие растворы называют также переохлажденными. В них что-то мешает началу кристаллизации, например, раствор слишком вязкий или для роста кристаллов требуются большие зародыши, которых в растворе нет.
Легко переохлаждаются растворы тиосульфата натрия Na 2 S 2 O 3 . 5H 2 O. Если осторожно нагреть кристаллы этого вещества примерно до 56° С, они «расплавятся». В действительности это не плавление, а растворение тиосульфата натрия в «собственной» кристаллизационной воде. С повышением температуры растворимость тиосульфата натрия, как и большинства других веществ, увеличивается, и при 56° С его кристаллизационной воды оказывается достаточно, чтобы растворить всю имеющуюся соль. Если теперь осторожно, избегая резких толчков, охладить сосуд, кристаллы не образуются и вещество останется жидким. Но если в переохлажденный раствор внести готовый зародыш – маленький кристаллик этого же вещества, то начнется быстрая кристаллизация. Интересно, что ее вызывает кристалл только этого вещества, а к постороннему раствор может быть совершенно безразличен. Поэтому если прикоснуться небольшим кристалликом тиосульфата к поверхности раствора, произойдет настоящее чудо: от кристаллика побежит фронт кристаллизации, который быстро дойдет до дна сосуда. Так что уже через несколько секунд жидкость полностью «затвердеет». Сосуд можно даже перевернуть – из него не выльется ни одной капли! Твердый тиосульфат можно снова расплавить в горячей воде и повторить все сначала.
Если пробирку с переохлажденным раствором тиосульфата поставить в ледяную воду, кристаллы будут расти медленнее, а сами будут крупнее. Кристаллизация пересыщенного раствора сопровождается его нагреванием – это выделяется тепловая энергия, полученная кристаллогидратом при его плавлении.
Тиосульфат натрия – не единственное вещество, образующее переохлажденный раствор, в котором можно вызвать быструю кристаллизацию. Подобным свойством обладает, например, и ацетат натрия CH 3 COONa (его легко получить действием уксусной кислоты на соду). С ацетатом натрия опытные лекторы демонстрируют такое «чудо»: на небольшую горку ацетата в блюдце они медленно льют пересыщенный раствор этой соли, который, соприкасаясь с кристаллами, немедленно кристаллизуется, образуя столбик твердой соли!
Кристаллы широко применяются в науке и технике: полупроводники, призмы и линзы для оптических приборов, твердотельные лазеры, пьезоэлектрики, сегнетоэлектрики, оптические и электрооптические кристаллы, ферромагнетики и ферриты, монокристаллы металлов высокой чистоты...
Рентгеноструктурные исследования кристаллов позволили установить строение многих молекул, в том числе и биологически активных – белков, нуклеиновых кислот.
Ограненные кристаллы драгоценных камней, в том числе выращенных искусственно, используются как украшения.
Илья Леенсон
Одним из самых распространенных материалов, с которым всегда предпочитали работать люди, был металл. В каждую эпоху предпочтение отдавалось разным видам этих удивительных веществ. Так, IV-III тысячелетия до нашей эры считаются веком хальколита, или медным. Позже его сменяет бронзовый, а затем в силу вступает тот, что и по сей день является актуальным - железный.
Сегодня вообще сложно представить, что когда-то можно было обходиться без металлических изделий, ведь практически все, начиная от предметов быта, медицинских инструментов и заканчивая тяжелой и легкой техникой, состоит из этого материала или включает в свой состав отдельные части из него. Почему же металлы сумели завоевать такую популярность? В чем проявляются особенности и как это заложено в их строении, попробуем разобраться далее.
Общее понятие о металлах
"Химия. 9 класс" - это учебник, по которому проходят обучение школьники. Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Именно с этого возраста рекомендуют давать детям представление о данных атомах и их свойствах, ведь подростки уже вполне могут оценить значение подобных знаний. Они прекрасно видят, что окружающее их разнообразие предметов, машин и прочих вещей имеет в своей основе как раз металлическую природу.
Что же такое металл? С точки зрения химии, к данным атомам принято относить те, что имеют:
- малое на внешнем уровне;
- проявляют сильные восстановительные свойства;
- имеют большой атомный радиус;
- как простые вещества обладают рядом специфических физических свойств.
Основу знаний об этих веществах можно получить, если рассмотреть атомно-кристаллическое строение металлов. Именно оно объясняет все особенности и свойства данных соединений.
В периодической системе для металлов отводится большая часть всей таблицы, ведь они образуют все побочные подгруппы и главные с первой по третью группу. Поэтому их численное превосходство очевидно. Самыми распространенными являются:
- кальций;
- натрий;
- титан;
- железо;
- магний;
- алюминий;
- калий.
Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет именно кристаллическое строение металлов.

Свойства металлов
К специфическим свойствам рассматриваемых веществ относят следующие.
- Металлический блеск. Все представители простых веществ им обладают, причем большинство одинаковым Лишь некоторые (золото, медь, сплавы) отличаются.
- Ковкость и пластичность - способность деформироваться и восстанавливаться достаточно легко. У разных представителей выражена в неодинаковой мере.
- Электропроводность и теплопроводность - одно из основных свойств, которое определяет области применения металла и его сплавов.
Кристаллическое строение металлов и сплавов объясняет причину каждого из обозначенных свойств и говорит о выраженности их у каждого конкретного представителя. Если знать особенности такого строения, то можно влиять на свойства образца и подстраивать его под нужные параметры, что и делают люди уже многие десятилетия.

Атомно-кристаллическое строение металлов
В чем же заключается такое строение, чем характеризуется? Само название говорит о том, что все металлы представляют собой кристаллы в твердом состоянии, то есть при обычных условиях (кроме ртути, которая является жидкостью). А что такое кристалл?
Это условное графическое изображение, построенное путем пересечения воображаемых линий через атомы, которые выстраивают тело. Другими словами, каждый металл состоит из атомов. Они располагаются в нем не хаотично, а очень правильно и последовательно. Так вот, если мысленно соединить все эти частицы в одну структуру, то получится красивое изображение в виде правильного геометрического тела какой-либо формы.
Это и принято называть кристаллической решеткой металла. Она очень сложная и пространственно объемная, поэтому для упрощения показывают не всю ее, а лишь часть, элементарную ячейку. Совокупность таких ячеек, собранная вместе и отраженная в и образует кристаллические решетки. Химия, физика и металловедение - это науки, которые занимаются изучением особенностей строения таких структур.

Сама - это набор атомов, которые располагаются на определенном расстоянии друг от друга и координируют вокруг себя строго фиксированное число других частиц. Она характеризуется плотностью упаковки, расстоянием между составными структурами, координационным числом. В целом все эти параметры являются характеристикой и всего кристалла, а значит, отражают и проявляемые металлом свойства.
Существует несколько разновидностей Объединяет их все одна особенность - в узлах находятся атомы, а внутри располагается облако электронного газа, которое формируется путем свободного передвижения электронов внутри кристалла.
Типы кристаллических решеток
Четырнадцать вариантов строения решетки принято объединять в три основных типа. Они следующие:
- Объемно-центрированная кубическая.
- Гексагональная плотноупакованная.
- Гранецентрированная кубическая.
Кристаллическое строение металлов было изучено только благодаря когда стало возможным получать большие увеличения изображений. А классификацию типов решеток впервые привел французский ученый Браве, по фамилии которого их иногда называют.

Объемно-центрированная решетка
Строение кристаллической решетки металлов данного типа представляет собой следующую структуру. Это куб, в узлах которого находится восемь атомов. Еще один располагается в центре свободного внутреннего пространства ячейки, что и объясняет название "объемно-центрированная".
Это один из вариантов наиболее простого строения элементарной ячейки, а значит, и всей решетки в целом. Такой тип имеют следующие металлы:
- молибден;
- ванадий;
- хром;
- марганец;
- альфа-железо;
- бетта-железо и другие.
Основные свойства таких представителей - высокая степень ковкости и пластичности, твердость и прочность.
Гранецентрированная решетка
Кристаллическое строение металлов, имеющих гранецентрированную кубическую решетку, представляет собой следующую структуру. Это куб, который включает в свой состав четырнадцать атомов. Восемь из них формируют узлы решетки, а еще шесть расположены по одному на каждой грани.
Подобную структуру имеют:
- алюминий;
- никель;
- свинец;
- гамма-железо;
- медь.
Основные отличительные свойства - блеск разного цвета, легкость, прочность, ковкость, повышенная устойчивость к коррозии.

Гексагональная решетка
Кристаллическое строение металлов, обладающих решетки, следующее. В основе элементарной ячейки лежит шестигранная призма. В ее узлах располагается 12 атомов, еще два по основаниям и три атома свободно лежат внутри пространства в центре структуры. Всего семнадцать атомов.
Подобную сложную конфигурацию имеют такие металлы, как:
- альфа-титан;
- магний;
- альфа-кобальт;
- цинк.
Основные свойства - высокая степень прочности, сильный серебристый блеск.
Дефекты кристаллического строения металлов
Однако все рассмотренные типы ячеек могут иметь и естественные недостатки, или так называемые дефекты. Это может быть связано с разными причинами: посторонними атомами и примесями в металлах, внешними воздействиями и прочим.
Поэтому существует классификация, отражающая дефекты, которые могут иметь кристаллические решетки. Химия как наука изучает каждый из них с целью выявления причины и способа устранения, чтобы свойства материала не были изменены. Итак, дефекты следующие.
- Точечные. Они бывают трех основных видов: вакансии, примеси или дислоцированные атомы. Приводят к ухудшению магнитных свойств металла, электро- и теплопроводности его.
- Линейные, или дислокационные. Выделяют краевые и винтовые. Ухудшают прочность и качество материала.
- Поверхностные дефекты. Влияют на внешний вид и структуру металлов.
В настоящее время разработаны методики устранения дефектов и получения чистых кристаллов. Однако совсем искоренить их не удается, идеальной кристаллической решетки не существует.

Значение знаний о кристаллическом строении металлов
Из вышеизложенного материала очевидно, что знания о тонкой структуре и строении позволяют спрогнозировать свойства материала и повлиять на них. И это позволяет делать наука химия. 9 класс общеобразовательной школы делает в процессе обучения упор на то, чтобы сформировать у учащихся четкое понятие о важном значении основополагающей логической цепочки: состав - строение - свойства - применение.
Сведения о кристаллическом строении металлов очень четко иллюстрирует и позволяет учителю наглядно объяснить и показать детям, насколько важно знать тонкую структуру, чтобы правильно и грамотно использовать все свойства.

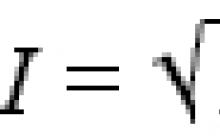








«плюсы» и«минусы» демократии
Геодезист. Кто такой геодезист? Описание профессии. Профессия геодезист Геодезист обучение
Магеллановы облака: кто они?
Перечный соус для стейка Сливочный перечный соус
Как составить грамотное портфолио дизайнеру