Кислоты - сложные вещества, состоящие из одного или нескольких атомов водорода, способных замещаться на атома металлов, и кислотных остатков.
Классификация кислот
1. По числу атомов водорода: число атомов водорода (n ) определяет основность кислот:
n = 1 одноосновная
n = 2 двухосновная
n = 3 трехосновная
2. По составу:
а) Таблица кислород содержащих кислот, кислотных остатков и соответствующих кислотных оксидов:
|
Кислота (Н n А) |
Кислотный остаток (А) |
Соответствующий кислотный оксид |
|
H 2 SO 4 серная |
SO 4 (II) сульфат |
SO 3 оксид серы (VI ) |
|
HNO 3 азотная |
NO 3 (I) нитрат |
N 2 O 5 оксид азота (V ) |
|
HMnO 4 марганцевая |
MnO 4 (I) перманганат |
Mn 2 O 7 оксид марганца (VII ) |
|
H 2 SO 3 сернистая |
SO 3 (II) сульфит |
SO 2 оксид серы (IV ) |
|
H 3 PO 4 ортофосфорная |
PO 4 (III) ортофосфат |
P 2 O 5 оксид фосфора (V ) |
|
HNO 2 азотистая |
NO 2 (I) нитрит |
N 2 O 3 оксид азота (III ) |
|
H 2 CO 3 угольная |
CO 3 (II) карбонат |
CO 2 оксид углерода (IV ) |
|
H 2 SiO 3 кремниевая |
SiO 3 (II) силикат |
SiO 2 оксид кремния (IV) |
|
НСlO хлорноватистая |
СlO (I) гипохлорит |
С l 2 O оксид хлора (I) |
|
НСlO 2 хлористая |
СlO 2 (I) хлорит |
С l 2 O 3 оксид хлора (III) |
|
НСlO 3 хлорноватая |
СlO 3 (I) хлорат |
С l 2 O 5 оксид хлора (V) |
|
НСlO 4 хлорная |
СlO 4 (I) перхлорат |
С l 2 O 7 оксид хлора (VII) |
б) Таблица бескислородных кислот
|
Кислота (Н n А) |
Кислотный остаток (А) |
|
HCl соляная, хлороводородная |
Cl (I ) хлорид |
|
H 2 S сероводородная |
S (II ) сульфид |
|
HBr бромоводородная |
Br (I ) бромид |
|
HI йодоводородная |
I (I ) йодид |
|
HF фтороводородная,плавиковая |
F (I ) фторид |
Физические свойства кислот
Многие кислоты, например серная, азотная, соляная – это бесцветные жидкости. известны также твёрдые кислоты: ортофосфорная, метафосфорная HPO 3 , борная H 3 BO 3 . Почти все кислоты растворимы в воде. Пример нерастворимой кислоты – кремниевая H 2 SiO 3 . Растворы кислот имеют кислый вкус. Так, например, многим плодам придают кислый вкус содержащиеся в них кислоты. Отсюда названия кислот: лимонная, яблочная и т.д.
Способы получения кислот
|
бескислородные |
кислородсодержащие |
|
HCl, HBr, HI, HF, H 2 S |
HNO 3 , H 2 SO 4 и другие |
|
ПОЛУЧЕНИЕ |
|
|
1. Прямое взаимодействие неметаллов H 2 + Cl 2 = 2 HCl |
1. Кислотный оксид + вода = кислота SO 3 + H 2 O = H 2 SO 4 |
|
2. Реакция обмена между солью и менее летучей кислотой 2 NaCl (тв .) + H 2 SO 4 (конц .) = Na 2 SO 4 + 2HCl |
|
Химические свойства кислот
1. Изменяют окраску индикаторов
|
Название индикатора |
Нейтральная среда |
Кислая среда |
|
Лакмус |
Фиолетовый |
Красный |
|
Фенолфталеин |
Бесцветный |
Бесцветный |
|
Метилоранж |
Оранжевый |
Красный |
|
Универсальная индикаторная бумага |
Оранжевая |
Красная |
2.Реагируют с металлами в ряду активности до H 2
(искл. HNO 3 –азотная кислота)
Видео "Взаимодействие кислот с металлами"
Ме + КИСЛОТА =СОЛЬ + H 2 (р. замещения)
Zn + 2 HCl = ZnCl 2 + H 2
3. С основными (амфотерными) оксидами – оксидами металлов
Видео "Взаимодействие оксидов металлов с кислотами"
Ме х О у + КИСЛОТА= СОЛЬ + Н 2 О (р. обмена)
4. Реагируют с основаниями – реакция нейтрализации
КИСЛОТА + ОСНОВАНИЕ= СОЛЬ+ H 2 O (р. обмена)
H 3 PO 4 + 3 NaOH = Na 3 PO 4 + 3 H 2 O
5. Реагируют с солями слабых, летучих кислот - если образуется кислота, выпадающая в осадок или выделяется газ:
2 NaCl (тв .) + H 2 SO 4 (конц .) = Na 2 SO 4 + 2HCl ( р . обмена )
Видео "Взаимодействие кислот с солями"
6. Разложение кислородсодержащих кислот при нагревании
(искл. H 2 SO 4 ; H 3 PO 4 )
КИСЛОТА = КИСЛОТНЫЙ ОКСИД + ВОДА (р. разложения)
Запомните! Неустойчивые кислоты (угольная и сернистая) – разлагаются на газ и воду :
H 2 CO 3 ↔ H 2 O + CO 2
H 2 SO 3 ↔ H 2 O + SO 2
Сероводородная кислота в продуктах выделяется в виде газа:
СаS + 2HCl = H 2 S + Ca Cl 2
ЗАДАНИЯ ДЛЯ ЗАКРЕПЛЕНИЯ
№1. Распределите химические формулы кислот в таблицу. Дайте им названия:
LiOH , Mn 2 O 7 , CaO , Na 3 PO 4 , H 2 S , MnO , Fe (OH ) 3 , Cr 2 O 3 ,HI , HClO 4 , HBr , CaCl 2 , Na 2 O , HCl , H 2 SO 4 , HNO 3 , HMnO 4 , Ca (OH ) 2 , SiO 2 , Кислоты
Бес-кисло-
родные
Кислород- содержащие
растворимые
нераст-воримые
одно-
основные
двух-основные
трёх-основные
№2. Составьте уравнения реакций:
Ca + HCl
Na + H 2 SO 4
Al + H 2 S
Ca
+ H 3 PO 4
Назовите продукты реакции.
№3. Составьте уравнения реакций, назовите продукты:
Na 2 O + H 2 CO 3
ZnO + HCl
CaO + HNO 3
Fe 2 O 3 + H 2 SO 4
№4. Составьте уравнения реакций взаимодействия кислот с основаниями и солями:
KOH + HNO 3
NaOH + H 2 SO 3
Ca(OH) 2 + H 2 S
Al(OH) 3 + HF
HCl + Na 2 SiO 3
H 2 SO 4 + K 2 CO 3
HNO 3 + CaCO 3
Назовите продукты реакции.
ТРЕНАЖЁРЫ
Тренажёр №1. "Формулы и названия кислот"
Тренажёр №2. " Установление соответствия: формула кислоты - формула оксида"
Техника безопасности - Оказание первой помощи при попадании кислот на кожу
Техника безопасности -
| Кислота | Кислотный остаток | ||
| Формула | Название | Формула | Название |
| HBr | бромоводородная | Br – | бромид |
| HBrO 3 | бромноватая | BrO 3 – | бромат |
| HCN | циановодородная (синильная) | CN – | цианид |
| HCl | хлороводородная (соляная) | Cl – | хлорид |
| HClO | хлорноватистая | ClO – | гипохлорит |
| HClO 2 | хлористая | ClO 2 – | хлорит |
| HClO 3 | хлорноватая | ClO 3 – | хлорат |
| HClO 4 | хлорная | ClO 4 – | перхлорат |
| H 2 CO 3 | угольная | HCO 3 – | гидрокарбонат |
| CO 3 2– | карбонат | ||
| H 2 C 2 O 4 | щавелевая | C 2 O 4 2– | оксалат |
| CH 3 COOH | уксусная | CH 3 COO – | ацетат |
| H 2 CrO 4 | хромовая | CrO 4 2– | хромат |
| H 2 Cr 2 O 7 | дихромовая | Cr 2 O 7 2– | дихромат |
| HF | фтороводородная (плавиковая) | F – | фторид |
| HI | иодоводородная | I – | иодид |
| HIO 3 | иодноватая | IO 3 – | иодат |
| H 2 MnO 4 | марганцовистая | MnO 4 2– | манганат |
| HMnO 4 | марганцовая | MnO 4 – | перманганат |
| HNO 2 | азотистая | NO 2 – | нитрит |
| HNO 3 | азотная | NO 3 – | нитрат |
| H 3 PO 3 | фосфористая | PO 3 3– | фосфит |
| H 3 PO 4 | фосфорная | PO 4 3– | фосфат |
| HSCN | тиоциановодородная (роданистая) | SCN – | тиоцианат (роданид) |
| H 2 S | сероводородная | S 2– | сульфид |
| H 2 SO 3 | сернистая | SO 3 2– | сульфит |
| H 2 SO 4 | серная | SO 4 2– | сульфат |
Окончание прил.
Приставки, наиболее часто употребляемые в названиях
Интерполяция справочных величин
Иногда необходимо узнать величину плотности или концентрации, не указанную в справочных таблицах. Искомый параметр можно найти методом интерполяции.
Пример
Для приготовления раствора HCl была взята имеющаяся в лаборатории кислота, плотность которой была определена ареометром. Она оказалась равной 1,082 г/см 3 .
По таблице справочника находим, что кислота плотностью 1,080 имеет массовую долю 16,74 %, а с 1,085 - 17,45 %. Чтобы найти массовую долю кислоты в имеющемся растворе, воспользуемся формулой для интерполяции:
![]() %,
%,
где индекс 1 относится к более разбавленному раствору, а 2 - к более концентрированному.
Предисловие……………………………..………….……….…......3
1. Основные понятия титриметрических методов анализа……...7
2. Методы и способы титрования……………………….....……...9
3. Вычисление молярной массы эквивалентов.…………………16
4. Способы выражения количественного состава растворов
в титриметрии……………………………………………………..21
4.1. Решение типовых задач на способы выражения
количественного состава растворов……………….……25
4.1.1. Расчет концентрации раствора по известным массе и объему раствора………………………………………..26
4.1.1.1. Задачи для самостоятельного решения...29
4.1.2. Пересчет одной концентрации в другую………...30
4.1.2.1. Задачи для самостоятельного решения...34
5. Способы приготовления растворов…………………………...36
5.1. Решение типовых задач на приготовление растворов
различными способами…………………………………..39
5.2. Задачи для самостоятельного решения………………….48
6. Расчет результатов титриметрического анализа………..........51
6.1. Расчет результатов прямого и заместительного
титрования………………………………………………...51
6.2. Расчет результатов обратного титрования……………...56
7. Метод нейтрализации (кислотно-основное титрование)……59
7.1. Примеры решения типовых задач…...…………………..68
7.1.1. Прямое и заместительное титрование……………68
7.1.1.1. Задачи для самостоятельного решения…73
7.1.2. Обратное титрование……………………………..76
7.1.2.1. Задачи для самостоятельного решения…77
8. Метод окисления-восстановления (редоксиметрия)………...80
8.1. Задачи для самостоятельного решения………………….89
8.1.1. Окислительно-восстановительные реакции……..89
8.1.2. Расчет результатов титрования…………………...90
8.1.2.1. Заместительное титрование……………...90
8.1.2.2. Прямое и обратное титрование…………..92
9. Метод комплексообразования; комплексонометрия…...........94
9.1. Примеры решения типовых задач……………………...102
9.2. Задачи для самостоятельного решения………………...104
10. Метод осаждения………………………………………........106
10.1. Примеры решения типовых задач…………………….110
10.2. Задачи для самостоятельного решения……………….114
11. Индивидуальные задания по титриметрическим
методам анализа…………………………………………………117
11.1. План выполнения индивидуального задания………...117
11.2. Варианты индивидуальных заданий………………….123
Ответы к задачам ………..………………………………………124
Условные обозначения……………………………………….…127
Приложение……………………………………………………...128
УЧЕБНОЕ ИЗДАНИЕ
АНАЛИТИЧЕСКАЯ ХИМИЯ
Кислотами называются сложные вещества, в состав молекул которых входят атомы водорода, способные замещаться или обмениваться на атомы металла и кислотный остаток.
По наличию или отсутствию кислорода в молекуле кислоты делятся на кислородсодержащие (H 2 SO 4 серная кислота, H 2 SO 3 сернистая кислота, HNO 3 азотная кислота, H 3 PO 4 фосфорная кислота, H 2 CO 3 угольная кислота, H 2 SiO 3 кремниевая кислота) и бескислородные (HF фтороводородная кислота, HCl хлороводородная кислота (соляная кислота), HBr бромоводородная кислота, HI иодоводородная кислота, H 2 S сероводородная кислота).
В зависимости от числа атомов водорода в молекуле кислоты кислоты бывают одноосновные (с 1 атомом Н), двухосновные (с 2 атомами Н) и трехосновные (с 3 атомами Н). Например, азотная кислота HNO 3 одноосновная, так как в молекуле её один атом водорода, серная кислота H 2 SO 4 – двухосновная и т.д.
Неорганических соединений, содержащих четыре атома водорода, способных замещаться на металл, очень мало.
Часть молекулы кислоты без водорода называется кислотным остатком.
Кислотные остатки могут состоять из одного атома (-Cl, -Br, -I) – это простые кислотные остатки, а могут – из группы атомов (-SO 3, -PO 4, -SiO 3) – это сложные остатки.
В водных растворах при реакциях обмена и замещения кислотные остатки не разрушаются:
H 2 SO 4 + CuCl 2 → CuSO 4 + 2 HCl
Слово ангидрид означает безводный, то есть кислота без воды. Например,
H 2 SO 4 – H 2 O → SO 3 . Бескислородные кислоты ангидридов не имеют.
Своё название кислоты получают от названия образующего кислоту элемента (кислотообразователя) с прибавлением окончаний «ная» и реже «вая»: H 2 SO 4 – серная; H 2 SO 3 – угольная; H 2 SiO 3 – кремниевая и т.д.
Элемент может образовать несколько кислородных кислот. В таком случае указанные окончания в названии кислот будут тогда, когда элемент проявляет высшую валентность (в молекуле кислоты большое содержание атомов кислорода). Если элемент проявляет низшую валентность, окончание в названии кислоты будет «истая»: HNO 3 – азотная, HNO 2 – азотистая.
Кислоты можно получать растворением ангидридов в воде. В случае, если ангидриды в воде не растворимы, кислоту можно получить действием другой более сильной кислоты на соль необходимой кислоты. Этот способ характерен как для кислородных так и бескислородных кислот. Бескислородные кислоты получают так же прямым синтезом из водорода и неметалла с последующим растворением полученного соединения в воде:
H 2 + Cl 2 → 2 HCl;
H 2 + S → H 2 S.
Растворы полученных газообразных веществ HCl и H 2 S и являются кислотами.
При обычных условиях кислоты бывают как в жидком, так и в твёрдом состоянии.
Химические свойства кислот
Растворыв кислот действуют на индикаторы. Все кислоты (кроме кремниевой) хорошо растворяются в воде. Специальные вещества – индикаторы позволяют определить присутствие кислоты.
Индикаторы – это вещества сложного строения. Они меняют свою окраску в зависимоти от взаимодействия с разными химическими веществами. В нейтральных растворах - они имеют одну окраску, в растворах оснований – другую. При взаимодействии с кислотой они меняют свою окраску: индикатор метиловый оранжевый окрашивается в красный цвет, индикатор лакмус – тоже в красный цвет.
Взаимодействуют с основаниями с образованием воды и соли, в которой содержится неизменный кислотный остаток (реакция нейтрализации):
H 2 SO 4 + Ca(OH) 2 → CaSO 4 + 2 H 2 O.
Взаимодействуют с основанными оксидами с образованием воды и соли (реакция нейтрализации). Соль содержит кислотный остаток той кислоты, которая использовалась в реакции нейтрализации:
H 3 PO 4 + Fe 2 O 3 → 2 FePO 4 + 3 H 2 O.
 Взаимодействуют с металлами.
Для взаимодействия кислот с металлами должны выполнятся некоторые условия:
Взаимодействуют с металлами.
Для взаимодействия кислот с металлами должны выполнятся некоторые условия:
1. металл должен быть достаточно активным по отношению к кислотам (в ряду активности металлов он должен располагаться до водорода). Чем левее находится металл в ряду активности, тем интенсивнее он взаимодействует с кислотами;
2. кислота должна быть достаточно сильной (то есть способной отдавать ионы водорода H +).
При протекании химических реакций кислоты с металлами образуется соль и выделяется водород (кроме взаимодействия металлов с азотной и концентрированной серной кислотами,):
Zn + 2HCl → ZnCl 2 + H 2 ;
Cu + 4HNO 3 → CuNO 3 + 2 NO 2 + 2 H 2 O.
Остались вопросы? Хотите знать больше о кислотах?
Чтобы получить помощь репетитора – зарегистрируйтесь .
Первый урок – бесплатно!
сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.
| Формулы кислот | Названия кислот | Названия соответствующих солей |
| HClO 4 | хлорная | перхлораты |
| HClO 3 | хлорноватая | хлораты |
| HClO 2 | хлористая | хлориты |
| HClO | хлорноватистая | гипохлориты |
| H 5 IO 6 | иодная | периодаты |
| HIO 3 | иодноватая | иодаты |
| H 2 SO 4 | серная | сульфаты |
| H 2 SO 3 | сернистая | сульфиты |
| H 2 S 2 O 3 | тиосерная | тиосульфаты |
| H 2 S 4 O 6 | тетратионовая | тетратионаты |
| HNO 3 | азотная | нитраты |
| HNO 2 | азотистая | нитриты |
| H 3 PO 4 | ортофосфорная | ортофосфаты |
| HPO 3 | метафосфорная | метафосфаты |
| H 3 PO 3 | фосфористая | фосфиты |
| H 3 PO 2 | фосфорноватистая | гипофосфиты |
| H 2 CO 3 | угольная | карбонаты |
| H 2 SiO 3 | кремниевая | силикаты |
| HMnO 4 | марганцовая | перманганаты |
| H 2 MnO 4 | марганцовистая | манганаты |
| H 2 CrO 4 | хромовая | хроматы |
| H 2 Cr 2 O 7 | дихромовая | дихроматы |
| HF | фтороводородная (плавиковая) | фториды |
| HCl | хлороводородная (соляная) | хлориды |
| HBr | бромоводородная | бромиды |
| HI | иодоводородная | иодиды |
| H 2 S | сероводородная | сульфиды |
| HCN | циановодородная | цианиды |
| HOCN | циановая | цианаты |
Напомню кратко на конкретных примерах, как следует правильно называть соли.
Пример 1 . Соль K 2 SO 4 образована остатком серной кислоты (SO 4) и металлом К. Соли серной кислоты называются сульфатами. K 2 SO 4 - сульфат калия.
Пример 2 . FeCl 3 - в состав соли входит железо и остаток соляной кислоты (Cl). Название соли: хлорид железа (III). Обратите внимание: в данном случае мы не только должны назвать металл, но и указать его валентность (III). В прошлом примере в этом не было необходимости, т. к. валентность натрия постоянна.
Важно: в названии соли следует указывать валентность металла только в том случае, если данный металл имеет переменную валентность!
Пример 3 . Ba(ClO) 2 - в состав соли входит барий и остаток хлорноватистой кислоты (ClO). Название соли: гипохлорит бария. Валентность металла Ва во всех его соединениях равна двум, указывать ее не нужно.
Пример 4 . (NH 4) 2 Cr 2 O 7 . Группа NH 4 называется аммоний, валентность этой группы постоянна. Название соли: дихромат (бихромат) аммония.
В приведенных выше примерах нам встретились только т. н. средние или нормальные соли. Кислые, основные, двойные и комплексные соли, соли органических кислот здесь обсуждаться не будут.
Если вас интересует не только номенклатура солей, но и методы их получения и химические свойства, рекомендую обратиться к соответствующим разделам справочника по химии: "
Названия некоторых неорганических кислот и солей
| Формулы кислот | Названия кислот | Названия соответствующих солей |
| HClO 4 | хлорная | перхлораты |
| HClO 3 | хлорноватая | хлораты |
| HClO 2 | хлористая | хлориты |
| HClO | хлорноватистая | гипохлориты |
| H 5 IO 6 | иодная | периодаты |
| HIO 3 | иодноватая | иодаты |
| H 2 SO 4 | серная | сульфаты |
| H 2 SO 3 | сернистая | сульфиты |
| H 2 S 2 O 3 | тиосерная | тиосульфаты |
| H 2 S 4 O 6 | тетратионовая | тетратионаты |
| H NO 3 | азотная | нитраты |
| H NO 2 | азотистая | нитриты |
| H 3 PO 4 | ортофосфорная | ортофосфаты |
| H PO 3 | метафосфорная | метафосфаты |
| H 3 PO 3 | фосфористая | фосфиты |
| H 3 PO 2 | фосфорноватистая | гипофосфиты |
| H 2 CO 3 | угольная | карбонаты |
| H 2 SiO 3 | кремниевая | силикаты |
| HMnO 4 | марганцовая | перманганаты |
| H 2 MnO 4 | марганцовистая | манганаты |
| H 2 CrO 4 | хромовая | хроматы |
| H 2 Cr 2 O 7 | дихромовая | дихроматы |
| HF | фтороводородная (плавиковая) | фториды |
| HCl | хлороводородная (соляная) | хлориды |
| HBr | бромоводородная | бромиды |
| HI | иодоводородная | иодиды |
| H 2 S | сероводородная | сульфиды |
| HCN | циановодородная | цианиды |
| HOCN | циановая | цианаты |
Напомню кратко на конкретных примерах, как следует правильно называть соли.
Пример 1 . Соль K 2 SO 4 образована остатком серной кислоты (SO 4) и металлом К. Соли серной кислоты называются сульфатами. K 2 SO 4 - сульфат калия.
Пример 2 . FeCl 3 - в состав соли входит железо и остаток соляной кислоты (Cl). Название соли: хлорид железа (III). Обратите внимание: в данном случае мы не только должны назвать металл, но и указать его валентность (III). В прошлом примере в этом не было необходимости, т. к. валентность натрия постоянна.
Важно: в названии соли следует указывать валентность металла только в том случае, если данный металл имеет переменную валентность!
Пример 3 . Ba(ClO) 2 - в состав соли входит барий и остаток хлорноватистой кислоты (ClO). Название соли: гипохлорит бария. Валентность металла Ва во всех его соединениях равна двум, указывать ее не нужно.
Пример 4 . (NH 4) 2 Cr 2 O 7 . Группа NH 4 называется аммоний, валентность этой группы постоянна. Название соли: дихромат (бихромат) аммония.
В приведенных выше примерах нам встретились только т. н. средние или нормальные соли. Кислые, основные, двойные и комплексные соли, соли органических кислот здесь обсуждаться не будут.

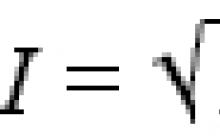








«плюсы» и«минусы» демократии
Геодезист. Кто такой геодезист? Описание профессии. Профессия геодезист Геодезист обучение
Магеллановы облака: кто они?
Перечный соус для стейка Сливочный перечный соус
Как составить грамотное портфолио дизайнеру