Водород
Водород – первый элемент и один из двух представителей I периода Периодической системы. Атом водорода состоит из двух частиц – протона и электрона, между которыми существуют лишь силы притяжения. Водород и металлы IА-группы проявляют степень окисления +1, являются восстановителями и имеют сходство оптических спектров. Однако в состоянии однозарядного катиона Н + (протона) водород не имеет аналогов. Кроме того, энергия ионизации атома водорода намного больше энергии ионизации атомов щелочных металлов.
С другой стороны, как у водорода, так и у галогенов не хватает одного электрона до завершения внешнего электронного слоя. Подобно галогенам, водород проявляет степень окисления –1 и окислительные свойства. Сходен водород с галогенами и по агрегатному состоянию, и по составу молекул Э 2 . Но молекулярная орбиталь (МО) Н 2 не имеет ничего общего с таковыми молекул галогенов, в то же время МО Н 2 имеет определенное сходство с МО двухатомных молекул щелочных металлов, существующих в парообразном состоянии.
Водород – самый распространенный элемент Вселенной, составляет основную массу Солнца, звезд и других космических тел. На Земле по распространенности занимает 9-е место; в свободном состоянии встречается редко, и основная часть его входит в состав воды, глин, каменного и бурого угля, нефти и т. д., а также сложных веществ живых организмов.
Природный водород представляет собой смесь стабильных изотопов протия 1 Н (99,985%) и дейтерия 2 H (2 D), радиоактивного трития 3 Н (3 Т).
Простые вещества. Возможны молекулы легкого водорода – Н 2 (дипротий), тяжелого водорода – D 2 (дидейтерий), Т 2 (дитритий), HD (протодейтерий), НТ (прототритий), DТ (дейтеротритий).
Н 2 (диводород, дипротий) – бесцветный трудносжижаемый газ, очень мало растворяется в воде, лучше – в органических растворителях, хемосорбируется металлами (Fe, Ni, Pt, Pd). В обычных условиях сравнительно мало активен и непосредственно взаимодействует лишь со фтором; при повышенных температурах реагирует с металлами, неметаллами, оксидами металлов. Особенно высока восстановительная способность у атомарного водорода Н 0 , образующегося при термическом разложении молекулярного водорода или в результате реакций непосредственно в зоне проведения восстановительного процесса.
Восстановительные свойства водород проявляет при взаимодействии с неметаллами, оксидами металлов, галогенидами:
Н 2 0 + Cl 2 = 2Н +1 Cl; 2Н 2 + О 2 = 2Н 2 О; СuО + Н 2 = Сu + Н 2 О
В качестве окислителя водород взаимодействует с активными металлами:
2Nа + Н 2 0 = 2NаН –1
Получение и применение водорода. В промышленности водород получают главным образом из природных и попутных газов, продуктов газификации топлива и коксового газа. Производство водорода основано на каталитических реакциях взаимодействия с водяным паром (конверсии) соответственно углеводородов (главным образом метана) и оксида углерода (II):
СН 4 + Н 2 О = СО + 3Н 2 (кат. Ni, 800°С)
СО + Н 2 О = СО 2 + Н 2 (кат. Fe, 550°С)
Важным способом получения водорода является выделение его из коксового газа и газов нефтепереработки путем глубокого охлаждения. Электролиз воды (электролитом обычно служит водный раствор щелочи) обеспечивает получение наиболее чистого водорода.
В лабораторных условиях водород обычно получают действием цинка на растворы серной или хлороводородной кислоты:
Zn + Н 2 SO 4 = ZnSO 4 + Н 2
Водород используется в химической промышленности для синтеза аммиака, метанола, хлороводорода, для гидрогенизации твердого и жидкого топлива, жиров и т. д. В виде водяного газа (в смеси с СО) применяется как топливо. При горении водорода в кислороде возникает высокая температура (до 2600°С), позволяющая сваривать и разрезать тугоплавкие металлы, кварц и пр. Жидкий водород используют как одно из наиболее эффективных реактивных топлив.
Соединения водорода (–I). Соединения водорода с менее электроотрицательными элементами, в которых он отрицательно поляризован относятся к гидридам , т.е. в основном его соединения с металлами.
В простых солеобразных гидридах существует анион Н – . Наиболее полярная связь наблюдается в гидридах активных металлов – щелочных и щелочно-земельных (например, КН, СаН 2). В химическом отношении ионные гидриды ведут себя как оснóвные соединения.
LiН + Н 2 О = LiОН + Н 2
К ковалентным относятся гидриды менее электроотрицательных, чем сам водород, неметаллических элементов (например, гидриды состава SiH 4 и ВН 3). По химической природе гидриды неметаллов являются кислотными соединениями.
SiH 4 + 3Н 2 О = Н 2 SiO 3 + 4Н 2
При гидролизе оснóвные гидриды образуют щелочь, а кислотные – кислоту.
Многие переходные металлы образуют гидриды с преимущественно металлическим характером связи нестехиометрического состава. Идеализированный состав металлических гидридов чаще всего отвечает формулам: М +1 Н (VН, NbН, ТаН), М +2 Н 2 (TiН 2 , ZrH 2) и М +3 Н 3 (UН 3 , РаН 3).
Соединения водорода (I). Положительная поляризация атомов водорода наблюдается в его многочисленных соединениях с ковалентной связью. При обычных условиях – это газы (НCl, Н 2 S, Н 3 N), жидкости (Н 2 О, НF, НNO 3), твердые вещества (Н 3 РO 4 , Н 2 SiO 3). Свойства этих соединений сильно зависят от природы электроотрицательного элемента.
Литий
Литий достаточно широко распространен в земной коре. Он входит в состав многих минералов, содержится в каменном угле, почвах, морской воде, а также в живых организмах. Наиболее ценны минералы – сподумен LiAl(SiО 3) 2 , амблигонит LiAl(PО 4)F и лепидолит Li 2 Al 2 (SiО 3) 3 (F,OH) 2 .
Простое вещество. Li (литий) – серебристо-белый, мягкий, низкоплавкий щелочной металл самый легкий из металлов. Реакционноспособный; на воздухе покрывается оксидно-нитридной пленкой (Li 2 О, Li 3 N). Воспламенятся при умеренном нагревании (выше 200°С); окрашивает пламя газовой горелки в темно-красный цвет. Сильный восстановитель. По сравнению с натрием и собственно щелочными металлами (подгруппа калия) литий является химически менее активным металлом. В обычных условиях бурно реагирует со всеми галогенами. При нагревании непосредственно соединяется с серой, углем, водородом и другими неметаллами. Будучи накален, горит в СО 2 . С металлами литий образует интерметаллические соединения. Кроме того, образует твердые растворы с Na, Al, Zn и с некоторыми другими металлами. Литий энергично разлагает воду, выделяя из нее водород, еще легче взаимодействует с кислотами.
2Li + Н 2 О = 2LiОН + Н 2
2Li + 2НCl = 2LiСl + Н 2
3Li + 4НNO 3 (разб.) = 2LiNO 3 + NO + 2Н 2 O
Литий хранят под слоем вазелина или парафина в запаянных сосудах.
Получение и применение. Литий получают при вакуум-термическом восстановлении сподумена или оксида лития в качестве восстановителя применяют кремний или алюминий.
2Li 2 О + Si = 4Li + SiО 2
3Li 2 О + 2Al = 6Li + A1 2 О 3
При электролитическом восстановлении используют расплав эвтектической смеси LiCl-KCl.
Литий придает сплавам ряд ценных физико-химических свойств. Так, у сплавов алюминия с содержанием до 1% Li повышается механическая прочность и коррозионная стойкость, введение 2% Li в техническую медь значительно увеличивает ее электрическую проводимость и т. д. Важнейшей областью применения лития является атомная энергетика (в качестве теплоносителя в атомных реакторах). Его используют как источник получения трития (3 Н).
Соединения лития (I). Бинарные соединения лития – бесцветные кристаллические вещества; являются солями или солеподобными соединениями. По химической природе, растворимости и характеру гидролиза они напоминают производные кальция и магния. Плохо растворимы LiF, Li 2 CО 3 , Li 3 PО 4 и др.
Пероксидные соединения для лития малохарактерны. Однако для него известны пероксид Li 2 О 2 , персульфид Li 2 S 2 и перкарбид Li 2 C 2 .
Оксид лития Li 2 О – оснóвный оксид, получается взаимодействием простых веществ. Активно реагирует с водой, кислотами, кислотными и амфотерными оксидами.
Li 2 О + Н 2 О = 2LiOH
Li 2 О + 2НCl(разб.) = 2LiCl + H 2 О
Li 2 О + CО 2 = Li 2 CО 3
Гидроксид лития LiOH – сильное основание, но по растворимости и силе уступает гидроксидам остальных щелочных металлов, и в отличие от них, при накаливании LiOH разлагается:
2LiOH ↔ Li 2 О + Н 2 О (800-1000°С, в атмосфере Н 2)
LiOH получают электролизом водных растворов LiCl. Применяется как электролит в аккумуляторах.
При совместной кристаллизации или сплавлении солей лития с однотипными соединениями других щелочных металлов образуются эвтектические смеси (LiNО 3 –KNО 3 и др.); реже образуются двойные соединения, например M +1 LiSО 4 , Na 3 Li(SО 4) 2 ∙6H 2 О и твердые растворы.
Расплавы солей лития и их смесей являются неводными растворителями; в них растворяется большинство металлов. Эти растворы имеют интенсивную окраску и являются очень сильными восстановителями. Растворение металлов в расплавленных солях важно для многих электрометаллургических и металлотермических процессов, для рафинирования металлов, проведения различных синтезов.
Натрий
Натрий – один из наиболее распространенных элементов на Земле. Важнейшие минералы натрия: каменная соль или галит NaCl, мирабилит или глауберова соль Na 2 SO 4 ∙10H 2 О, криолит Na 3 AlF 6 , бура Na 2 B 4 O 7 ∙10H 2 О и др.; входит в состав многих природных силикатов и алюмосиликатов. Соединения натрия содержатся в гидросфере (около 1,5∙10 т), в живых организмах (так, в крови человека ионы Na + составляют 0,32%, в мышечной ткани – до 1,5%).
Простое вещество. Na (натрий) – серебристо-белый, легкий, очень мягкий, низкоплавкий щелочной металл. Весьма реакционноспособный; на воздухе покрывается оксидной пленкой (тускнеет), воспламеняется при умеренном нагревании. Устойчив в атмосфере аргона и азота (с азотом реагирует только при нагревании). Сильный восстановитель; энергично реагирует с водой, кислотами, неметаллами. С ртутью образует амальгаму (в отличие от чистого натрия, реакция с водой протекает спокойно). Окрашивает пламя газовой горелки в желтый цвет.
2Na + Н 2 О = 2NaOH + Н 2
2Na + 2НCl(разб.) = 2NaCl + Н 2
2Na + 2NaOH(ж) = 2Na 2 О + H 2
2Na + H 2 = 2NaH
2Na + Hal 2 = 2NaHal (комн., Hal = F, Cl; 150-200° C, Hal = Br, I)
2Na + NH 3 (г) = 2NaNH 2 + H 2
Co многими металлами натрий образует интерметаллические соединения. Так, с оловом дает ряд соединений: NaSn 6 , NaSn 4 , NaSn 3 , NaSn 2 , NaSn, Na 2 Sn, Na 3 Sn и др.; с некоторыми металлами дает твердые растворы.
Натрий хранят в запаянных сосудах или под слоем керосина.
Получение и применение натрия. Натрий получают электролизом расплавленного NaCl и реже NaOH. При электролитическом восстановлении NaCl используют эвтектическую смесь, например, NaCl-KCl (температура плавления почти на 300°С ниже, чем температура плавления NaCl).
2NaCl(ж) = 2Na + Cl 2 (эл. ток)
Натрий используется в металлотермии, органическом синтезе, ядерных энергетических установках (в качестве теплоносителя), клапанах авиационных двигателей, химических производствах, где требуется равномерный обогрев в пределах 450-650° С.
Соединения натрия (I). Наиболее характерны ионные соединения кристаллического строения, отличающиеся тугоплавкостью, хорошо растворяются в воде. Труднорастворимы некоторые производные со сложными анионами, как гексагидроксостибат (V) Na; мало растворим NaHCO 3 (в отличие от карбоната).
При взаимодействии с кислородом натрий (в отличие от лития) образует не оксид, а пероксид: 2Na + O 2 = Na 2 O 2
Оксид натрия Na 2 O получают восстановлением Na 2 O 2 металлическим натрием. Известны также малостойкие озонид NaO 3 и надпероксид натрия NaO 2 .
Из соединений натрия важное значение имеют его хлорид, гидроксид, карбонаты и многочисленные другие производные.
Хлорид натрия NaCl является основой для целого ряда важнейших производств, таких, как производство натрия, едкого натра, соды, хлора и др.
Гидроксид натрия (едкий натр, каустическая сода ) NaOH – очень сильное основание. Применяется в разнообразных отраслях промышленности, главные из которых – производство мыл, красок, целлюлозы и др. Получают NaOH электролизом водных растворов NaCl и химическими методами. Так, распространен известковый способ – взаимодействие раствора карбоната натрия (соды) с гидроксидом кальция (гашеной известью):
Na 2 CO 3 + Са(ОН) 2 = 2NaOH + СаСO 3
Карбонаты натрия Na 2 CO 3 (кальцинированная сода ), Na 2 СО 3 ∙10Н 2 О (кристаллическая сода ), NaHCO 3 (питьевая сода ) используются в химической, мыловаренной, бумажной, текстильной, пищевой промышленности.
Подгруппа калия (калий, рубидий, цезий, франций)
Элементы подгруппы калия – наиболее типичные металлы. Для них наиболее характерны соединения с преимущественно ионным типом связи. Комплексообразование с неорганическими лигандами для К + , Rb + , Cs + нехарактерно.
Наиболее важными минералами калия являются: сильвин КCl, сильвинит NaCl∙KCl, карналлит KCl∙MgCl 2 ∙6H 2 О, каинит KCl∙MgSО 4 ∙3H 2 О. Калий (вместе с натрием) входит в состав живых организмов и всех силикатных пород. Рубидий и цезий содержатся в минералах калия. Франций радиоактивен, стабильных изотопов не имеет (наиболее долгоживущий изотоп Fr с периодом полураспада 22 мин.).
Простые вещества. К (калий) – серебристо-белый, мягкий, низкоплавкий щелочной металл. Чрезвычайно реакционноспособный, сильнейший восстановитель; реагирует с О 2 воздуха, водой (идет воспламенение выделяющегося Н 2), разбавленными кислотами, неметаллами, аммиаком, сероводородом, расплавом гидроксида калия. Практически не реагирует с азотом (в отличие от лития и натрия). Образует интерметаллиды с Na, Tl, Sn, Pb и Bi. Окрашивает пламя газовой горелки в фиолетовый цвет.
Rb (рубидий) – белый, мягкий, весьма низкоплавкий щелочной металл. Чрезвычайно реакционноспособный; сильнейший восстановитель; энергично реагирует с О 2 воздуха, водой (идет воспламенение металла и выделяющегося Н 2), разбавленными кислотами, неметаллами, аммиаком, сероводородом. Не реагирует с азотом. Окрашивает пламя газовой горелки в фиолетовый цвет.
Cs (цезий) – белый (на срезе светло-желтый), мягкий, весьма низкоплавкий щелочной металл. Чрезвычайно реакционноспособный, сильнейший восстановитель; реагирует с О 2 воздуха, водой (идет воспламенение металла и выделяющегося Н 2), разбавленными кислотами, неметаллами, аммиаком, сероводородом. He реагирует с азотом. Окрашивает пламя газовой горелки в синий цвет.
Fr (франций) – белый, весьма легкоплавкий щелочной металл. Радиоактивен. Самый реакционноспособный из всех металлов, по химическому поведению подобен цезию. На воздухе покрывается оксидной пленкой. Сильный восстановитель; энергично реагирует с водой и кислотами, выделяя Н 2 . Выделены соединения франция FrClО 4 и Fr 2 методом осаждения с соответствующими малорастворимыми солями Rb и Cs.
Калий и его аналоги хранят в запаянных сосудах, а также под слоем парафинового или вазелинового масла. Калий, кроме того, хорошо сохраняется под слоем керосина или бензина.
Получение и применение. Калий получают электролизом расплава КCl и натрийтермическим методом из расплавленного гидроксида или хлорида калия. Рубидий и цезий чаще получают вакуум-термическим восстановлением их хлоридов металлическим кальцием. Все щелочные металлы хорошо очищаются возгонкой в вакууме.
Металлы подгруппы калия при нагревании и освещении сравнительно легко теряют электроны, и эта способность делает их ценным материалом для изготовления фотоэлементов.
Соединения калия (I), рубидия (I), цезия (I). Производные калия и его аналогов являются преимущественно солями и солеподобными соединениями. По составу, кристаллическому строению, растворимости и характеру сольволиза их соединения проявляют большое сходство с однотипными соединениями натрия.
В соответствии с усилением химической активности в ряду K–Rb–Cs возрастает тенденция к образованию пероксидных соединений. Так, при сгорании они образуют надпероксиды ЭО 2 . Косвенным путем можно получить также пероксиды Э 2 О 2 и озониды ЭО 3 . Пероксиды, надпероксиды и озониды – сильные окислители, легко разлагаются водой и разбавленными кислотами:
2КО 2 + 2Н 2 О = 2КОН + Н 2 О 2 + О 2
2КО 2 + 2НCl = 2КCl + Н 2 О 2 + О 2
4КО 3 + 2Н 2 О = 4КОН + 5О 2
Гидроксиды ЭОН – самые сильные основания (щелочи); при накаливании, подобно NaOH, возгоняются без разложения. При растворении в воде выделяется значительное количество теплоты. Наибольшее значение в технике имеет КОН (едкое кали), получаемый электролизом водного раствора КCl.
В противоположность аналогичным соединениям Li + и Na + их оксохлораты (VII) ЭОCl 4 , хлороплатинаты (IV) Э 2 РlCl 6 , нитритокобальтаты (III) Э 3 [Со(NO 2) 6 ] и некоторые другие труднорастворимы.
Из производных подгруппы наибольшее значение имеют соединения калия. Около 90% солей калия потребляется в качестве удобрении. Его соединения применяются также в производстве стекла, мыла.
Подгруппа меди (медь, серебро, золото)
Для меди наиболее характерны соединения со степенями окисления +1 и +2, для золота +1 и +3, а для серебра +1. Все они обладают ярко выраженной склонностью к комплексообразованию.
Все элементы IB-группы относятся к сравнительно малораспространенным. Наибольшее значение из природных соединений меди имеют минералы: медный колчедан (халькопирит ) CuFeS 2 , медный блеск Cu 2 S, а также куприт Cu 2 О, малахит CuСО 3 ∙Cu(ОН) 2 и др. Серебро входит в состав сульфидных минералов других металлов (Pd, Zn, Cd и др.). Для Cu, Ag и Au довольно обычны также арсенидные, стибидные и сульфидарсенидные минералы. Медь, серебро и особенно золото встречаются в природе в самородном состоянии.
Все растворимые соединения меди, серебра и золота ядовиты.
Простые вещества. Си (медь) – красный, мягкий, ковкий металл. Не изменяется на воздухе в отсутствии влаги и СO 2 , при нагревании тускнеет (образование оксидной пленки). Слабый восстановитель (благородный металл); не реагирует с водой. Переводится в раствор кислотами-неокислителями или гидратом аммиака в присутствии O 2 , цианидом калия. Окисляется концентрированными серной и азотной кислотами, «царской водкой», кислородом, галогенами, халькогенами, оксидами металлов. Реагирует при нагревании с галогеноводородами.
Cu + H 2 SO 4 (конц., гор.) = CuSО 4 + SO 2 + H 2 O
Cu + 4НNO 3 (конц.) = Cu(NO 3) 2 + 2NO 2 + 2H 2 O
ЗCu + 8НNO 3 (разб.) = 3Cu(NO 3) 2 + 2NO + 4Н 2 O
2Cu + 4НCl(разб.) + O 2 = 2CuCl 2 + 2Н 2 O
Cu + Cl 2 (влаж., комн.) = CuCl 2
2Cu + O 2 (нагр.) = 2CuО
Cu + 4KCN(конц.) + Н 2 O = 2K + 2KOH + H 2
4Cu + 2O 2 + 8NH 3 + 2Н 2 O = 4OH
2Cu + СO 2 + O 2 + Н 2 O = Cu 2 СO 3 (ОН) 2 ↓
Ag (серебро) – белый, тяжелый, пластичный металл. Малоактивный (благородный металл); не реагирует с кислородом, водой, разбавленными хлороводородной и серной кислотами. Слабый восстановитель; реагирует с кислотами-окислителями. Чернеет в присутствии влажного H 2 S.
Ag + 2H 2 SO 4 (конц., гор.) = Ag 2 SO 4 ↓ + SO 2 + Н 2 O
3Ag + 4HNO 3 (paзб.) = 3AgNO 3 + NO + 2H 2 O
4Ag + H 2 S + О 2 (воздух) = 2Ag 2 S + 2H 2 O
2Ag + Наl 2 (нагр.) = 2AgHal
4Ag + 8KCN + 2H 2 O + O 2 = 4K + 4KOH
Аи (золото) – желтый, ковкий, тяжелый, высокоплавкий металл. Устойчив в сухом и влажном воздухе. Благородный металл; не реагирует с водой, кислотами-неокислителями, концентрированной серной и азотной кислотами, щелочами, гидратом аммиака, кислородом, азотом, углеродом, серой. В растворе простых катионов не образует. Переводится в раствор «царской водкой» , смесями галогенов и галогеноводородных кислот, кислородом в присутствии цианидов щелочных металлов. Окисляется нитратом натрия при сплавлении, дифторидом криптона.
Au + HNO 3 (конц.) + 4НCl(конц.) = Н + NO + 2Н 2 O
2Au + 6H 2 SeO 4 (конц., гор.) = Au 2 (SeO 4) 3 + 3SeO 2 + 6Н 2 O
2Au + 3Cl 2 (до 150°C) = 2AuCl 3
2Au + Cl 2 (150-250°С) = 2AuCl
Au + 3Наl + 2ННаl(конц.) = Н + NO + 2Н 2 О (Hal = Cl, Br, I)
4Au + 8NaCN + 2Н 2 О + О 2 = 4Na + 4KOH
Au + NaN0 3 = NaAuО 2 + NO
Получение и применение. Медь получают пирометаллургическим восстановлением окисленных сульфидных концентратов. Выделяющийся при обжиге сульфидов диоксид серы SO 2 идет на производство серной кислоты, а шлак используется для производства шлакобетона, каменного литья, шлаковаты и пр. Восстановленную черновую медь очищают электрохимическим рафинированием. Из анодного шлама извлекают благородные металл, селен, теллур и др. Серебро получают при переработке полиметаллических (серебряно-свинцово-цинковых) сульфидных руд. После окислительного обжига, цинк отгоняют, медь окисляют, а черновое серебро подвергают электрохимическому рафинированию. При цианидном способе добычи золота сначала золотоносную породу отмывают водой, затем обрабатывают раствором NaCN на воздухе; при этом золото образует комплекс Na, из которого его осаждают цинком:
Na + Zn = Na 2 + 2Au↓
Этим способом можно выделять и серебро из бедных руд. При ртутном способе золотоносную породу обрабатывают ртутью с целью получения амальгамы золота, затем ртуть отгоняется.
Си, Ag и Au друг с другом и со многими другими металлами образуют сплавы. Из сплавов меди наибольшее значение имеют бронзы (90% Cu, 10% Sn), томпак (90% Cu, 10% Zn), мельхиор (68% Cu, 30% Ni, 1% Mn, 1% Fe), нейзильбер (65% Cu, 20% Zn, 15% Ni), латунь (60% Cu, 40% Zn), а также монетные сплавы.
Ввиду высокой тепло- и электропроводимости, ковкости, хороших литейных качеств, большого сопротивления на разрыв и химической стойкости медь широко используется в промышленности, электротехнике, машиностроении. Из меди изготавливают электрические провода и кабели, различную промышленную аппаратуру (котлы, перегонные кубы и т.п.)
Серебро и золото вследствие мягкости обычно сплавляют с другими металлами, чаще с медью. Сплавы серебра служат для изготовления ювелирных и бытовых изделий, монет, радиодеталей, серебряно-цинковых аккумуляторов, в медицине. Сплавы золота применяются для электрических контактов, для зубопротезирования, в ювелирном деле.
Соединения меди (I), серебра (I) и золота (I). Степень окисления +1 наиболее характерна для серебра; у меди и, в особенности, у золота эта степень окисления проявляется реже.
Бинарные соединения Cu (I), Ag (I) и Au (I) – твердые кристаллические солеподобные вещества, в большинстве нерастворимые в воде. Производные Ag (I) образуются при непосредственном взаимодействии простых веществ, а Cu (I) и Au (I) – при восстановлении соответствующих соединений Cu (II) и Au (III).
Для Cu (I) и Ag (I) устойчивы амминокомплексы типа [Э(NH 3) 2 ] + , и поэтому большинство соединений Cu (I) и Ag (I) довольно легко растворяется в присутствии аммиака, так:
CuCl + 2NH 3 = Cl
Ag 2 O + 4NH 3 + H 2 O = 2(OH)
Гидроксиды типа [Э(NH 3) 2 ](OH) значительно устойчивее, чем ЭОН, и по силе приближаются к щелочам. Гидроксиды ЭОН неустойчивы, и при попытке их получения по обменным реакциям выделяются оксиды CuО (красный), Ag 2 O (темно-коричневый), так:
2AgNO 3 + 2NaOH = Ag 2 O + 2NaNO 3 + Н 2 O
Оксиды Э 2 O проявляют кислотные свойства при взаимодействии с соответствующими основными соединениями образуются купраты (I), аргентаты (I) и аураты (I).
Cu 2 O + 2NаОН(конц.) + Н 2 O = 2Na
Нерастворимые в воде и кислотах галогениды ЭНаl довольно значительно растворяются в растворах галогеноводородных кислот или основных галогенидов:
CuCl + HC1 = H AgI + KI = K
Аналогично ведут себя нерастворимые в воде цианиды ЭCN, сульфиды Э 2 S и пр.
Большинство соединений Cu (I) и Au (I) легко окисляется (даже кислородом воздуха), переходя в устойчивые производные Cu (II) и Au (III).
4CuCl + O 2 + 4НCl = 4CuCl 2 + 2Н 2 О
Для соединений. Cu (I) и Au (I) характерно диспропорционирование:
2CuC1 = СuCl 2 + Cu
3AuCl + КCl = K + 2Au
Большинство соединений Э (I) при небольшом нагревании и при действии света легко распадаются, поэтому их обычно хранят в банках из темного стекла. Светочувствительность галогенидов серебра используется для приготовления светочувствительных эмульсий. Оксид меди (I) применяют для окрашивания стекла, эмалей, а также в полупроводниковой технике.
Соединения меди (II). Степень окисления +2 характерна только для меди. При растворении солей Cu (II) в воде или при взаимодействии CuО (черного цвета) и Cu(ОН) 2 (голубого цвета) с кислотами образуются голубые аквакомплексы 2+ . Такую же окраску имеет большинство кристаллогидратов, например, Cu(NO 3) 2 ∙6H 2 O; встречаются также кристаллогидраты Cu (II), имеющие зеленую и темно-коричневую окраску.
При действии аммиака на растворы солей меди (II) образуются аммиакаты:
Cu(OH) 2 ↓ + 4NH 3 + 2H 2 = (OH) 2
Для меди (II) характерны также анионные комплексы – купраты (II). Так, Сu(ОН) 2 при нагревании в концентрированных растворах щелочей частично растворяется, образуя синие гидроксокупраты (II) типа M 2 +1 . В водных растворах гидроксокупраты (II) легко разлагаются.
В избытке основных галогенидов CuHal 2 образуют галогенокупраты (II) типа M +1 и М 2 +1 [СuНаl 4 ]. Известны также анионные комплексы Cu (II) с цианид-, карбонат-, сульфат- и другими анионами.
Из соединений меди (II) технически наиболее важен кристаллогидрат CuSO 4 ∙5H 2 O (медный купорос ) применяется для получения красок, для борьбы с вредителями и болезнями растений, служит исходными продуктом для получения меди и ее соединений и т. д.
Соединения меди (III), серебра (III), золота (III). Степень окисления +3 наиболее характерна для золота. Соединения меди (III) и серебра (III) неустойчивы и являются сильными окислителями.
Исходным продуктом для получения многих соединений золота является АuCl 3 , который получают взаимодействием порошка Аu с избытком Cl 2 при 200°С.
Галогениды, оксид и гидроксид Au (III) – амфотерные соединения с преобладанием кислотных свойств.
NaOH + Au(OH) 3 = Na
Au(OH) 3 + 4HN0 3 = H + 3H 2 O
AuHal 3 + M +1 Hal = M
Нитрато- и цианоаураты (III) водорода выделены в свободном состоянии. В присутствии солей щелочных металлов образуются аураты, например: М +1 , M +1 и др.
Соединения золота (V) и(VII). Взаимодействием золота и фторида криптона (II) получен пентафторид золота AuF 5:
2Au + 5KrF 2 = 2AuF 5 + 5Кr
Пентафторид AuF 5 проявляет кислотные свойства, с оснóвными фторидами образует фтороаураты (V).
NaF + AuF 5 = Na
Соединения Au (V) – очень сильные окислители. Так, AuF 5 окисляет даже XeF 2:
AuF 5 + XeF 2 = XeF 4 + AuF 3
Известны также соединения типа XeFAuF 6 , XeF 5 AuF 6 и некоторые другие.
Известен крайне неустойчивый фторид AuF 7 .
Атом водорода имеет электронную формулу внешнего (и единственного) электронного уровня 1s 1 . С одной стороны, по наличию одного электрона на внешнем электронном уровне атом водорода похож на атомы щелочных металлов. Однако, ему, так же как и галогенам не хватает до заполнения внешнего электронного уровня всего одного электрона, поскольку на первом электронном уровне может располагаться не более 2-х электронов. Выходит, что водород можно поместить одновременно как в первую, так и в предпоследнюю (седьмую) группу таблицы Менделеева, что иногда и делается в различных вариантах периодической системы:
С точки зрения свойств водорода как простого вещества, он, все-таки, имеет больше общего с галогенами. Водород, также как и галогены, является неметаллом и образует аналогично им двухатомные молекулы (H 2).
В обычных условиях водород представляет собой газообразное, малоактивное вещество. Невысокая активность водорода объясняется высокой прочностью связи между атомами водорода в молекуле, для разрыва которой требуется либо сильное нагревание, либо применение катализаторов, либо и то и другое одновременно.
Взаимодействие водорода с простыми веществами
с металлами
Из металлов водород реагирует только с щелочными и щелочноземельными! К щелочным металлам относятся металлы главной подгруппы I-й группы (Li, Na, K, Rb, Cs, Fr), а к щелочно-земельным — металлы главной подгруппы II-й группы, кроме бериллия и магния (Ca, Sr, Ba, Ra)
При взаимодействии с активными металлами водород проявляет окислительные свойства, т.е. понижает свою степень окисления. При этом образуются гидриды щелочных и щелочноземельных металлов, которые имеют ионное строение. Реакция протекает при нагревании:
Следует отметить, что взаимодействие с активными металлами является единственным случаем, когда молекулярный водород Н 2 является окислителем.
с неметаллами
Из неметаллов водород реагирует только c углеродом, азотом, кислородом, серой, селеном и галогенами!
Под углеродом следует понимать графит или аморфный углерод, поскольку алмаз — крайне инертная аллотропная модификация углерода.
При взаимодействии с неметаллами водород может выполнять только функцию восстановителя, то есть только повышать свою степень окисления:
Взаимодействие водорода со сложными веществами
с оксидами металлов
Водород не реагирует с оксидами металлов, находящихся в ряду активности металлов до алюминия (включительно), однако, способен восстанавливать многие оксиды металлов правее алюминия при нагревании:
c оксидами неметаллов
Из оксидов неметаллов водород реагирует при нагревании с оксидами азота, галогенов и углерода. Из всех взаимодействий водорода с оксидами неметаллов особенно следует отметить его реакцию с угарным газом CO.
Смесь CO и H 2 даже имеет свое собственное название – «синтез-газ», поскольку из нее в зависимости от условий могут быть получены такие востребованные продукты промышленности как метанол, формальдегид и даже синтетические углеводороды:
c кислотами
С неорганическими кислотами водород не реагирует!
Из органических кислот водород реагирует только с непредельными, а также с кислотами, содержащими функциональные группы способные к восстановлению водородом, в частности альдегидные, кето- или нитрогруппы.
c солями
В случае водных растворов солей их взаимодействие с водородом не протекает. Однако при пропускании водорода над твердыми солями некоторых металлов средней и низкой активности возможно их частичное или полное восстановление, например:
Химические свойства галогенов
Галогенами называют химические элементы VIIA группы (F, Cl, Br, I, At), а также образуемые ими простые вещества. Здесь и далее по тексту, если не сказано иное, под галогенами будут пониматься именно простые вещества.
Все галогены имеют молекулярное строение, что обусловливает низкие температуры плавления и кипения данных веществ. Молекулы галогенов двухатомны, т.е. их формулу можно записать в общем виде как Hal 2 .
Следует отметить такое специфическое физическое свойство йода, как его способность к сублимации или, иначе говоря, возгонке . Возгонкой , называют явление, при котором вещество, находящееся в твердом состоянии, при нагревании не плавится, а, минуя жидкую фазу, сразу же переходит в газообразное состояние.
Электронное строение внешнего энергетического уровня атома любого галогена имеет вид ns 2 np 5 , где n – номер периода таблицы Менделеева, в котором расположен галоген. Как можно заметить, до восьмиэлектронной внешней оболочки атомам галогенов не хватает всего одного электрона. Из этого логично предположить преимущественно окисляющие свойства свободных галогенов, что подтверждается и на практике. Как известно, электроотрицательность неметаллов при движении вниз по подгруппе снижается, в связи с чем активность галогенов уменьшается в ряду:
F 2 > Cl 2 > Br 2 > I 2
Взаимодействие галогенов с простыми веществами
Все галогены являются высокоактивными веществами и реагируют с большинством простых веществ. Однако, следует отметить, что фтор из-за своей чрезвычайно высокой реакционной способности может реагировать даже с теми простыми веществами, с которыми не могут реагировать остальные галогены. К таким простым веществам относятся кислород, углерод (алмаз), азот, платина, золото и некоторые благородные газы (ксенон и криптон). Т.е. фактически, фтор не реагирует лишь с некоторыми благородными газами.
Остальные галогены, т.е. хлор, бром и йод, также являются активными веществами, однако менее активными, чем фтор. Они реагируют практически со всеми простыми веществами, кроме кислорода, азота, углерода в виде алмаза, платины, золота и благородных газов.
Взаимодействие галогенов с неметаллами
водородом
При взаимодействии всех галогенов с водородом образуются галогеноводороды с общей формулой HHal. При этом, реакция фтора с водородом начинается самопроизвольно даже в темноте и протекает со взрывом в соответствии с уравнением:
Реакция хлора с водородом может быть инициирована интенсивным ультрафиолетовым облучением или нагреванием. Также протекает со взрывом:
Бром и йод реагируют с водородом только при нагревании и при этом, реакция с йодом является обратимой:
фосфором
Взаимодействие фтора с фосфором приводит к окислению фосфора до высшей степени окисления (+5). При этом происходит образование пентафторида фосфора:
При взаимодействии хлора и брома с фосфором возможно получение галогенидов фосфора как в степени окисления + 3, так и в степени окисления +5, что зависит от пропорций реагирующих веществ:
При этом в случае белого фосфора в атмосфере фтора, хлора или жидком броме реакция начинается самопроизвольно.
Взаимодействие же фосфора с йодом может привести к образованию только триодида фосфора из-за существенно меньшей, чем у остальных галогенов окисляющей способности:
серой
Фтор окисляет серу до высшей степени окисления +6, образуя гексафторид серы:
Хлор и бром реагируют с серой, образуя соединения, содержащие серу в крайне не свойственных ей степенях окисления +1 и +2. Данные взаимодействия являются весьма специфичными, и для сдачи ЕГЭ по химии умение записывать уравнения этих взаимодействий не обязательно. Поэтому три нижеследующих уравнения даны скорее для ознакомления:
Взаимодействие галогенов с металлами
Как уже было сказано выше, фтор способен реагировать со всеми металлами, даже такими малоактивными как платина и золото:
Остальные галогены реагируют со всеми металлами кроме платины и золота:
Реакции галогенов со сложными веществами
Реакции замещения с галогенами
Более активные галогены, т.е. химические элементы которых расположены выше в таблице Менделеева, способны вытеснять менее активные галогены из образуемых ими галогеноводородных кислот и галогенидов металлов:
Аналогичным образом, бром и йод вытесняют серу из растворов сульфидов и или сероводорода:
Хлор является более сильным окислителем и окисляет сероводород в его водном растворе не до серы, а до серной кислоты:
Взаимодействие галогенов с водой
Вода горит во фторе синим пламенем в соответствии с уравнением реакции:
Бром и хлор реагируют с водой иначе, чем фтор. Если фтор выступал в роли окислителя, то хлор и бром диспропорционируют в воде, образуя смесь кислот. При этом реакции обратимы:
Взаимодействие йода с водой протекает в настолько ничтожно малой степени, что им можно пренебречь и считать, что реакция не протекает вовсе.
Взаимодействие галогенов с растворами щелочей
Фтор при взаимодействии с водным раствором щелочи опять же выступает в роли окислителя:
Умение записывать данное уравнение не требуется для сдачи ЕГЭ. Достаточно знать факт о возможности такого взаимодействия и окислительной роли фтора в этой реакции.
В отличие от фтора, остальные галогены в растворах щелочей диспропорционируют, то есть одновременно и повышают и понижают свою степень окисления. При этом, в случае хлора и брома в зависимости от температуры возможно протекание по двум разным направлениям. В частности, на холоду реакции протекают следующим образом:
а при нагревании:
Йод реагирует с щелочами исключительно по второму варианту, т.е. с образованием йодата, т.к. гипоиодит не устойчив не только при нагревании, но также при обычной температуре и даже на холоду.
Водород
ВОДОРО́Д -а; м. Химический элемент (H), лёгкий газ без цвета и запаха, образующий в соединении с кислородом воду.
◁ Водоро́дный, -ая, -ое. В-ые соединения. В-ые бактерии. В-ая бомба (бомба огромной разрушительной силы, взрывное действие которой основано на термоядерной реакции). Водоро́дистый, -ая, -ое.
водоро́д(лат. Hydrogenium), химический элемент VII группы периодической системы. В природе встречаются два стабильных изотопа (протий и дейтерий) и один радиоактивный (тритий). Молекула двухатомна (Н 2). Газ без цвета и запаха; плотность 0,0899 г/л, t кип - 252,76°C. Соединяется с многими элементами, с кислородом образует воду. Самый распространённый элемент космоса; составляет (в виде плазмы) более 70% массы Солнца и звёзд, основная часть газов межзвёздной среды и туманностей. Атом водорода входит в состав многих кислот и оснований, большинства органических соединений. Применяют в производстве аммиака, соляной кислоты, для гидрогенизации жиров и др., при сварке и резке металлов. Перспективен как горючее (см. Водородная энергетика).
ВОДОРОДВОДОРО́Д (лат. Hydrogenium), H, химический элемент с атомным номером 1, атомная масса 1,00794. Химический символ водорода Н читается в нашей стране «аш», как произносится эта буква по-французски.
Природный водород состоит из смеси двух стабильных нуклидов (см.
НУКЛИД)
с массовыми числами 1,007825 (99,985 % в смеси) и 2,0140 (0,015 %). Кроме того, в природном водороде всегда присутствуют ничтожные количества радиоактивного нуклида - трития (см.
ТРИТИЙ)
3 Н (период полураспада Т 1/2 12,43 года).
Так как в ядре атома водорода содержится только 1 протон (меньше в ядре атома элемента протонов быть не может), то иногда говорят, что водород образует естественную нижнюю границу периодической системы элементов Д. И. Менделеева (хотя сам элемент водород расположен в самой верхней части таблицы). Элемент водород расположен в первом периоде таблицы Менделеева. Его относят и к 1-й группе (группе IА щелочных металлов (см.
ЩЕЛОЧНЫЕ МЕТАЛЛЫ)
), и к 7-й группе (группе VIIA галогенов (см.
ГАЛОГЕНЫ)
).
Массы атомов у изотопов водорода различаются между собой очень сильно (в разы). Это приводит к заметным различиям в их поведении в физических процессах (дистилляция, электролиз и др.) и к определенным химическим различиям (различия в поведении изотопов одного элемента называют изотопными эффектами, для водорода изотопные эффекты наиболее существенны). Поэтому в отличие от изотопов всех остальных элементов изотопы водорода имеют специальные символы и названия. Водород с массовым числом 1 называют легким водородом, или протием (лат. Protium, от греческого protos - первый), обозначают символом Н, а его ядро называют протоном (см.
ПРОТОН (элементарная частица))
, символ р. Водород с массовым числом 2 называют тяжелым водородом, дейтерием (см.
ДЕЙТЕРИЙ)
(лат Deuterium, от греческого deuteros - второй), для его обозначения используют символs 2 Н, или D (читается «де»), ядро d - дейтрон. Радиоактивный изотоп с массовым числом 3 называют сверхтяжелым водородом, или тритием (лат. Tritum, от греческого tritos - третий), символ 2 Н или Т (читается «те»), ядро t - тритон.
Конфигурация единственного электронного слоя нейтрального невозбужденного атома водорода 1s
1
. В соединениях проявляет степени окисления +1 и, реже, –1 (валентность I). Радиус нейтрального атома водорода 0,024 нм. Энергия ионизации атома 13,595 эВ, сродство к электрону 0,75 эВ. По шкале Полинга электроотрицательность водорода 2,20. Водород принадлежит к числу неметаллов.
В свободном виде - легкий горючий газ без цвета, запаха и вкуса.
История открытия
Выделение горючего газа при взаимодействии кислот и металлов наблюдали в 16 и 17 веках на заре становления химии как науки. Знаменитый английский физик и химик Г. Кавендиш (см.
КАВЕНДИШ Генри)
в 1766 исследовал этот газ и назвал его «горючим воздухом». При сжигании «горючий воздух» давал воду, но приверженность Кавендиша теории флогистона (см.
ФЛОГИСТОН)
помешала ему сделать правильные выводы. Французский химик А. Лавуазье (см.
ЛАВУАЗЬЕ Антуан Лоран)
совместно с инженером Ж. Менье (см.
МЕНЬЕ Жан Батист Мари Шарль)
, используя специальные газометры, в 1783 осуществил синтез воды, а затем и ее анализ, разложив водяной пар раскаленным железом. Таким образом он установил, что «горючий воздух» входит в состав воды и может быть из нее получен. В 1787 Лавуазье пришел к выводу, что «горючий воздух» представляет собой простое вещество, и, следовательно, относится к числу химических элементов. Он дал ему название hydrogene (от греческого hydor - вода и gennao - рождаю) - «рождающий воду». Установление состава воды положило конец «теории флогистона». Русское наименование «водород» предложил химик М. Ф. Соловьев (см.
СОЛОВЬЕВ Михаил Федорович)
в 1824. На рубеже 18 и 19 веков было установлено, что атом водорода очень легкий (по сравнению с атомами других элементов), и вес (масса) атома водорода был принят за единицу сравнения атомных масс элементов. Массе атома водорода приписали значение, равное 1.
Нахождение в природе
На долю водорода приходится около 1% массы земной коры (10-е место среди всех элементов). В свободном виде водород на нашей планете практически не встречается (его следы имеются в верхних слоях атмосферы), но в составе воды распространен на Земле почти повсеместно. Элемент водород входит в состав органических и неорганических соединений живых организмов, природного газа, нефти, каменного угля. Он содержится, разумеется, в составе воды (около 11% по массе), в различных природных кристаллогидратах и минералах, в составе которых имеется одна или несколько гидроксогрупп ОН.
Водород как элемент доминирует во Вселенной. На его долю приходится около половины массы Солнца и других звезд, он присутствует в атмосфере ряда планет.
Получение
Водород можно получить многими способами. В промышленности для этого используют природные газы, а также газы, получаемые при переработке нефти, коксовании и газификации угля и других топлив. При производстве водорода из природного газа (основной компонент - метан) проводят его каталитическое взаимодействие с водяным паром и неполное окисление кислородом:
CH 4 + H 2 O = CO + 3H 2 и CH 4 + 1/2 O 2 = CO 2 + 2H 2
Выделение водорода из коксового газа и газов нефтепереработки основано на их сжижении при глубоком охлаждении и удалении из смеси газов, сжижаемых легче, чем водород. При наличии дешевой электроэнергии водород получают электролизом воды, пропуская ток через растворы щелочей. В лабораторных условиях водород легко получить взаимодействием металлов с кислотами, например, цинка с соляной кислотой.
Физические и химические свойства
При обычных условиях водород - легкий (плотность при нормальных условиях 0,0899 кг/м 3) бесцветный газ. Температура плавления –259,15 °C, температура кипения –252,7 °C. Жидкий водород (при температуре кипения) обладает плотностью 70,8 кг/м 3 и является самой легкой жидкостью. Стандартный электродный потенциал Н 2 /Н - в водном растворе принимают равным 0. Водород плохо растворим в воде: при 0 °C растворимость составляет менее 0,02 см 3 /мл, но хорошо растворим в некоторых металлах (губчатое железо и других), особенно хорошо - в металлическом палладии (около 850 объемов водорода в 1 объеме металла). Теплота сгорания водорода равна 143,06 МДж/кг.
Существует в виде двухатомных молекул Н 2 . Константа диссоциации Н 2 на атомы при 300 К 2,56·10 -34 . Энергия диссоциации молекулы Н 2 на атомы 436 кДж/моль. Межъядерное расстояние в молекуле Н 2 0,07414 нм.
Так как ядро каждого атома Н, входящего в состав молекулы, имеет свой спин (см.
СПИН)
, то молекулярный водород может находиться в двух формах: в форме ортоводорода (о-Н 2) (оба спина имеют одинаковую ориентацию) и в форме параводорода (п-Н 2) (спины имеют разную ориентацию). При обычных условиях нормальный водород представляет собой смесь 75% о-Н 2 и 25% п-Н 2 . Физические свойства п- и о-Н 2 немного различаются между собой. Так, если температура кипения чистого о-Н 2 20,45 К, то чистого п-Н 2 - 20,26 К. Превращение о-Н 2 в п-Н 2 сопровождается выделением 1418 Дж/моль теплоты.
В научной литературе неоднократно высказывались соображения о том, что при высоких давлениях (выше 10 ГПа) и при низких температурах (около 10 К и ниже) твердый водород, обычно кристаллизующийся в гексагональной решетке молекулярного типа, может переходить в вещество с металлическими свойствами, возможно, даже сверхпроводник. Однако пока однозначных данных о возможности такого перехода нет.
Высокая прочность химической связи между атомами в молекуле Н 2 (что, например, используя метод молекулярных орбиталей, можно объяснить тем, что в этой молекуле электронная пара находится на связывающей орбитали, а разрыхляющая орбиталь электронами не заселена) приводит к тому, что при комнатной температуре газообразный водород химически малоактивен. Так, без нагревания, при простом смешивании водород реагирует (со взрывом) только с газообразным фтором:
H 2 + F 2 = 2HF + Q.
Если смесь водорода и хлора при комнатной температуре облучить ультрафиолетовым светом, то наблюдается немедленное образование хлороводорода НСl. Реакция водорода с кислородом происходит со взрывом, если в смесь этих газов внести катализатор - металлический палладий (или платину). При поджигании смесь водорода и кислорода (так называемый гремучий газ (см.
ГРЕМУЧИЙ ГАЗ)
) взрывается, при этом взрыв может произойти в смесях, в которых содержание водорода составляет от 5 до 95 объемных процентов. Чистый водород на воздухе или в чистом кислороде спокойно горит с выделением большого количества теплоты:
H 2 + 1/2O 2 = Н 2 О + 285,75 кДж/моль
С остальными неметаллами и металлами водород если и взаимодействует, то только при определенных условиях (нагревание, повышенное давление, присутствие катализатора). Так, с азотом водород обратимо реагирует при повышенном давлении (20-30 МПа и больше) и при температуре 300-400 °C в присутствии катализатора - железа:
3H 2 + N 2 = 2NH 3 + Q.
Также только при нагревании водород реагирует с серой с образованием сероводорода H 2 S, с бромом - с образованием бромоводорода НBr, с иодом - с образованием иодоводорода НI. С углем (графитом) водород реагирует с образованием смеси углеводородов различного состава. С бором, кремнием, фосфором водород непосредственно не взаимодействует, соединения этих элементов с водородом получают косвенными путями.
При нагревании водород способен вступать в реакции с щелочными, щелочноземельными металлами и магнием с образованием соединений с ионным характером связи, в составе которых содержится водород в степени окисления –1. Так, при нагревании кальция в атмосфере водорода образуется солеобразный гидрид состава СаН 2 . Полимерный гидрид алюминия (AlH 3) x - один из самых сильных восстановителей - получают косвенными путями (например, с помощью алюминийорганических соединений). Со многими переходными металлами (например, цирконием, гафнием и др.) водород образует соединения переменного состава (твердые растворы).
Водород способен реагировать не только со многими простыми, но и со сложными веществами. Прежде всего надо отметить способность водорода восстанавливать многие металлы из их оксидов (такие, как железо, никель, свинец, вольфрам, медь и др.). Так, при нагревании до температуры 400-450 °C и выше происходит восстановление железа водородом из его любого оксида, например:
Fe 2 O 3 + 3H 2 = 2Fe + 3H 2 O.
Следует отметить, что восстановить водородом из оксидов можно только металлы, расположенные в ряду стандартных потенциалов за марганцем. Более активные металлы (в том числе и марганец) до металла из оксидов не восстанавливаются.
Водород способен присоединяться по двойной или тройной связи ко многим органическим соединениям (это - так называемые реакции гидрирования). Например, в присутствии никелевого катализатора можно осуществить гидрирование этилена С 2 Н 4 , причем образуется этан С 2 Н 6:
С 2 Н 4 + Н 2 = С 2 Н 6 .
Взаимодействием оксида углерода(II) и водорода в промышленности получают метанол:
2Н 2 + СО = СН 3 ОН.
В соединениях, в которых атом водорода соединен с атомом более электроотрицательного элемента Э (Э = F, Cl, O, N), между молекулами образуются водородные связи (см.
ВОДОРОДНАЯ СВЯЗЬ)
(два атома Э одного и того же или двух разных элементов связаны между собой через атом Н: Э"... Н... Э"", причем все три атома расположены на одной прямой). Такие связи существуют между молекулами воды, аммиака, метанола и др. и приводят к заметному возрастанию температур кипения этих веществ, увеличению теплоты испарения и т. д.
Применение
Водород используют при синтезе аммиака NH 3 , хлороводорода HCl, метанола СН 3 ОН, при гидрокрекинге (крекинге в атмосфере водорода) природных углеводородов, как восстановитель при получении некоторых металлов. Гидрированием (см.
ГИДРИРОВАНИЕ)
природных растительных масел получают твердый жир - маргарин. Жидкий водород находит применение как ракетное топливо, а также как хладагент. Смесь кислорода с водородом используют при сварке.
Одно время высказывалось предположение, что в недалеком будущем основным источником получения энергии станет реакция горения водорода, и водородная энергетика вытеснит традиционные источники получения энергии (уголь, нефть и др.). При этом предполагалось, что для получения водорода в больших масштабах можно будет использовать электролиз воды. Электролиз воды - довольно энергоемкий процесс, и в настоящее время получать водород электролизом в промышленных масштабах невыгодно. Но ожидалось, что электролиз будет основан на использовании среднетемпературной (500-600 °C) теплоты, которая в больших количествах возникает при работе атомных электростанций. Эта теплота имеет ограниченное применение, и возможности получения с ее помощью водорода позволили бы решить как проблему экологии (при сгорании водорода на воздухе количество образующихся экологически вредных веществ минимально), так и проблему утилизации среднетемпературной теплоты. Однако после Чернобыльской катастрофы развитие атомной энергетики повсеместно свертывается, так что указанный источник энергии становится недоступным. Поэтому перспективы широкого использования водорода как источника энергии пока сдвигаются по меньшей мере до середины 21-го века.
Особенности обращения
Водород не ядовит, но при обращении с ним нужно постоянно учитывать его высокую пожаро- и взрывоопасность, причем взрывоопасность водорода повышена из-за высокой способности газа к диффузии даже через некоторые твердые материалы. Перед началом любых операций по нагреванию в атмосфере водорода следует убедиться в его чистоте (при поджигании водорода в перевернутой вверх дном пробирке звук должен быть глухой, а не лающий).
Биологическая роль
Биологическое значение водорода определяется тем, что он входит в состав молекул воды и всех важнейших групп природных соединений, в том числе белков, нуклеиновых кислот, липидов, углеводов. Примерно 10 % массы живых организмов приходится на водород. Способность водорода образовывать водородную связь играет решающую роль в поддержании пространственной четвертичной структуры белков, а также в осуществлении принципа комплементарности (см.
КОМПЛЕМЕНТАРНОСТЬ)
в построении и функциях нуклеиновых кислот (то есть в хранении и реализации генетической информации), вообще в осуществлении «узнавания» на молекулярном уровне. Водород (ион Н +) принимает участие в важнейших динамических процессах и реакциях в организме - в биологическом окислении, обеспечивающим живые клетки энергией, в фотосинтезе у растений, в реакциях биосинтеза, в азотфиксации и бактериальном фотосинтезе, в поддержании кислотно-щелочного равновесия и гомеостаза (см.
ГОМЕОСТАЗ)
, в процессах мембранного транспорта. Таким образом, наряду с кислородом и углеродом водород образует структурную и функциональную основы явлений жизни.
Энциклопедический словарь . 2009 .
Синонимы :Смотреть что такое "водород" в других словарях:
Таблица нуклидов Общие сведения Название, символ Водород 4, 4H Нейтронов 3 Протонов 1 Свойства нуклида Атомная масса 4,027810(110) … Википедия
Таблица нуклидов Общие сведения Название, символ Водород 5, 5H Нейтронов 4 Протонов 1 Свойства нуклида Атомная масса 5,035310(110) … Википедия
Таблица нуклидов Общие сведения Название, символ Водород 6, 6H Нейтронов 5 Протонов 1 Свойства нуклида Атомная масса 6,044940(280) … Википедия
Таблица нуклидов Общие сведения Название, символ Водород 7, 7H Нейтронов 6 Протонов 1 Свойства нуклида Атомная масса 7,052750(1080) … Википедия
Водород был открыт во второй половине 18 столетия английским ученым в области физики и химии Г. Кавендишем. Он сумел выделить вещество в чистом состоянии, занялся его изучением и описал свойства.
Такова история открытия водорода. В ходе экспериментов исследователь определил, что это горючий газ, сгорание которого в воздухе дает воду. Это привело к определению качественного состава воды.
Что такое водород
О водороде, как о простом веществе, впервые заявил французский химик А. Лавуазье в 1784 году, поскольку определил, что в состав его молекулы входят атомы одного вида.

Название химического элемента по-латыни звучит как hydrogenium (читается «гидрогениум»), что означает «воду рождающий». Название отсылает к реакции горения, в результате которой образуется вода.
Характеристика водорода
Обозначение водорода Н. Менделеев присвоил этому химическому элементу первый порядковый номер, разместив его в главной подгруппе первой группы и первом периоде и условно в главной подгруппе седьмой группы.

Атомарный вес (атомная масса) водорода составляет 1,00797. Молекулярная масса H 2 равна 2 а. е. Молярная масса численно равна ей.
Представлен тремя изотопами, имеющими специальное название: самый распространенный протий (H), тяжелый дейтерий (D), радиоактивный тритий (Т).
Это первый элемент, который может быть полностью разделен на изотопы простым способом. Основывается он на высокой разнице масс изотопов. Впервые процесс был осуществлен в 1933 году. Объясняется это тем, что лишь в 1932 году был выявлен изотоп с массой 2.
Физические свойства
В нормальных условиях простое вещество водород в виде двухатомных молекул является газом, без цвета, у которого отсутствует вкус и запах. Мало растворим в воде и других растворителях.

Температура кристаллизации — 259,2 о C, температура кипения — 252,8 о C. Диаметр молекул водорода настолько мал, что они обладают способностью к медленной диффузии через ряд материалов (резина, стекло, металлы). Это свойство находит применение, когда требуется очистить водород от газообразных примесей. При н. у. водород имеет плотность, равную 0,09 кг/м3.
Возможно ли превращение водорода в металл по аналогии с элементами, расположенными в первой группе? Учеными установлено, что водород в условиях, когда давление приближается к 2 млн. атмосфер, начинает поглощать инфракрасные лучи, что свидетельствует о поляризации молекул вещества. Возможно, при еще более высоких давлениях, водород станет металлом.

Это интересно: есть предположение, что на планетах-гигантах, Юпитере и Сатурне, водород находится в виде металла. Предполагается, что в составе земного ядра тоже присутствует металлический твердый водород, благодаря сверхвысокому давлению, создаваемому земной мантией.
Химические свойства
В химическое взаимодействие с водородом вступают как простые, так и сложные вещества. Но малую активность водорода требуется увеличить созданием соответствующих условий – повышением температуры, применением катализаторов и др.

При нагревании в реакцию с водородом вступают такие простые вещества, как кислород (O 2), хлор(Cl 2), азот (N 2), сера(S).
Если поджечь чистый водород на конце газоотводной трубки в воздухе, он будет гореть ровно, но еле заметно. Если же поместить газоотводную трубку в атмосферу чистого кислорода, то горение продолжится с образованием на стенках сосуда капель воды, как результат реакции:

Горение воды сопровождается выделением большого количества теплоты. Это экзотермическая реакция соединения, в процессе которой водород окисляется кислородом с образованием оксида H 2 O. Это также и окислительно-восстановительная реакция, в которой водород окисляется, а кислород восстанавливается.
Аналогично происходит реакция с Cl 2 с образованием хлороводорода.

Для осуществления взаимодействия азота с водородом требуется высокая температура и повышенное давление, а также присутствие катализатора. Результатом является аммиак.

В результате реакции с серой образуется сероводород, распознавание которого облегчает характерный запах тухлых яиц.

Степень окисления водорода в этих реакциях +1, а в гидридах, описываемых ниже, – 1.
При реакции с некоторыми металлами образуются гидриды, например, гидрид натрия – NaH. Некоторые из этих сложных соединений используются в качестве горючего для ракет, а также в термоядерной энергетике.
Водород реагирует и с веществами из категории сложных. Например, с оксидом меди (II), формула CuO. Для осуществления реакции, водород меди пропускается над нагретым порошкообразным оксидом меди (II). В ходе взаимодействия реагент меняет свой цвет и становится красно-коричневым, а на холодных стенках пробирки оседают капельки воды.

Водород в ходе реакции окисляется, образуя воду, а медь восстанавливается из оксида до простого вещества (Cu).
Области применения

Водород имеет большое значение для человека и находит применение в самых разных сферах:
- В химическом производстве – это сырье, в других отраслях – топливо. Не обходятся без водорода и предприятия нефтехимии и нефтепереработки.
- В электроэнергетике это простое вещество выполняет функцию охлаждающего агента.
- В черной и цветной металлургии водороду отводится роль восстановителя.
- Сего помощью создают инертную среду при упаковке продуктов.
- Фармацевтическая промышленность — пользуется водородом как реагентом в производстве перекиси водорода.
- Этим легким газом наполняют метеорологические зонды.
- Известен этот элемент и в качестве восстановителя топлива для ракетных двигателей.
Ученые единодушно пророчат водородному топливу пальму первенства в энергетике.
Получение в промышленности
В промышленности водород получают методом электролиза, которому подвергают хлориды либо гидроксиды щелочных металлов, растворенные в воде. Также можно получать водород этим способом непосредственно из воды.

Используется в этих целях конверсия кокса или метана с водяным паром. Разложение метана при повышенной температуре также дает водород. Сжижение коксового газа фракционным методом тоже применяется для промышленного получения водорода.
Получение в лаборатории
В лаборатории для получения водорода используют аппарат Киппа.

В качестве реагентов выступают соляная или серная кислота и цинк. В результате реакции образуется водород.
Нахождение водорода в природе
Водород чаще других элементов встречается во Вселенной. Основную массу звезд, в том числе Солнца, и иных космических тел составляет водород.

В земной коре его всего 0,15%. Он присутствует во многих минералах, во всех органических веществах, а также в воде, покрывающей на 3/4 поверхность нашей планеты.
В верхних слоях атмосферы можно обнаружить следы водорода в чистом виде. Находят его и в ряде горючих природных газов.
Газообразный водород является самым неплотным, а жидкий – самым плотным веществом на нашей планете. С помощью водорода можно изменить тембр голоса, если вдохнуть его, а на выдохе заговорить.

В основе действия самой мощной водородной бомбы лежит расщепление самого легкого атома.
Водород является самым первым элементом в Периодической системе химических элементов, имеет атомный номер 1 и относительную атомную массу 1,0079. Каковы физические свойства водорода?
Физические свойства водорода
В переводе с латыни водород означает «рождающий воду». Еще в 1766 году английский ученый Г. Кавендиш собрал выделяющийся при действии кислот на металлы «горючий воздух» и стал исследовать его свойства. В 1787 году А. Лавуазье определил этот «горючий воздух» как новый химический элемент, который входит в состав воды.

Рис. 1. А. Лавуазье.
У водорода существуют 2 стабильных изотопа – протий и дейтерий, а также радиоактивный – тритий, количество которого на нашей планете очень мало.
Водород является самым распространенным элементом в космосе. Солнце и большинство звезд имеют водород в своем составе в качестве основного элемента. Также этот газ входит в состав воды, нефти, природного газа. Общее содержание водорода на Земле составляет 1%.

Рис. 2. Формула водорода.
В состав атома этого вещества входит ядро и один электрон. Когда у водорода теряется электрон, он образует положительно заряженный ион, то есть проявляет металлические свойства. Но также атом водорода способен не только терять, но и присоединять электрон. В этом он очень похож на галогены. Поэтому водород в Периодической системе относится и к I и к VII группе. Неметаллические свойства водорода выражены у него в большей степени.
Молекула водорода состоит из двух атомов, связанных между собой ковалентной связью
Водород при обычных условиях является бесцветным газообразным элементом, который не имеет запаха и вкуса. Он в 14 раз легче воздуха, а его температура кипения составляет -252,8 градусов по Цельсию.
Таблица «Физические свойства водорода»
Кроме физических свойств водород обладает и рядом химических свойств. водород при нагревании или под действием катализаторов вступает в реакции с металлами и неметаллами, серой, селеном, теллуром, а также может восстанавливать оксиды многих металлов.
Получение водорода
Из промышленных способов получения водорода (кроме электролиза водных растворов солей) следует отметить следующие:
- пропускание паров воды через раскаленный уголь при температуре 1000 градусов:
- конверсия метана водяным паром при температуре 900 градусов:
CH 4 +2H 2 O=CO 2 +4H 2

Рис. 3. Паровая конверсия метана.
- разложение метана в присутствии катализатора (Ni) при температуре 400 градусов:

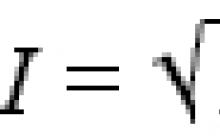








«плюсы» и«минусы» демократии
Геодезист. Кто такой геодезист? Описание профессии. Профессия геодезист Геодезист обучение
Магеллановы облака: кто они?
Перечный соус для стейка Сливочный перечный соус
Как составить грамотное портфолио дизайнеру